
科目: 来源: 题型:解答题
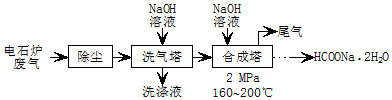
 .
.查看答案和解析>>
科目: 来源: 题型:实验题
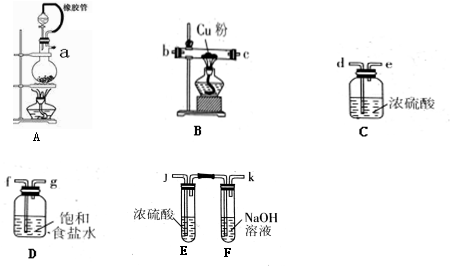
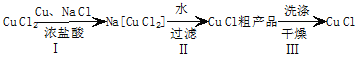
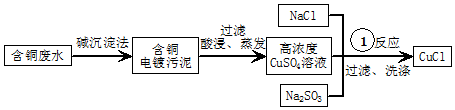
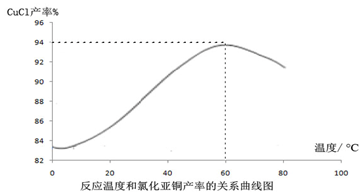
查看答案和解析>>
科目: 来源: 题型:选择题
| 化学式 | AgCl | Ag2CrO4 | CH3COOH | HClO | H2CO3 |
| Ksp或Ka | Ksp=1.8×10-10 | Ksp=2.0×10-12 | Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.1×10-7 Ka2=5.6×10-11 |
| A. | 向浓度均为1×10-4 mol/L的KCl和K2CrO4混合液中逐滴加入1×10-3 mol/LAgNO3溶液,CrO42-先沉淀(10-5 mol/L是否太小?这个浓度一般都认为沉淀完全了) | |
| B. | H2CO3、HCO3-、CH3COO-、ClO-在溶液中可以大量共存 | |
| C. | 相同浓度的CH3COONa和NaClO混合溶液,各离子浓度的大小关系为:c(Na+)>c(CH3COO-)>c(ClO-)>c(OH-)>c(H+) | |
| D. | 碳酸钠溶液中滴加少量氯水的离子方程式为:CO32-+Cl2+H2O═HCO3-+Cl-+HClO |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 简单阳离子的氧化性:A<C | |
| B. | 可用含氧酸的酸性比较B、D元素的非金属性 | |
| C. | 简单离子半径:C>D>E>B | |
| D. | A、C、E三种元素形成的化合物既还有离子键又含有共价键 |
查看答案和解析>>
科目: 来源: 题型:选择题
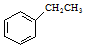 $→_{△}^{Fe_{2}O_{3}}$
$→_{△}^{Fe_{2}O_{3}}$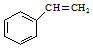 +H2,下列说法正确的是( )
+H2,下列说法正确的是( )| A. | 乙苯苯环上的一氯取代物有三种 | |
| B. | 1mol苯乙烯分别与足量的溴水或氢气反应最多消耗Br2或H24mol | |
| C. | 乙苯分子中共平面的碳原子最多只有7个 | |
| D. | 该反应为还原反应 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 实验操作 | 相应实验现象 | 结论或推论 | |
| A | 溴水中加入苯,充分振荡、静置 | 水层几乎呈无色 | 苯与溴发生了反应 |
| B | 一小粒金属钠投入装有无水乙醇的试管中 | 反应结束前一段时间,钠浮在乙醇表面 | 密度:乙醇大于钠 |
| C | 分别向盛有KI3溶液的a、b试管中滴加淀粉溶液和AgNO3溶液 | a中溶液变蓝,b中产生黄色沉淀 | KI3溶液中存在:I3-?I2+I- |
| D | 分别向含Mn2+的草酸溶液X和不含Mn2+的草酸溶液Y中滴加酸性高锰酸钾溶液 | 高锰酸钾溶液在X溶液中褪色较快 | Mn2+也能还原高锰酸钾 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1mol蔗糖完全水解生成葡萄糖分子数为2 NA | |
| B. | 在氢氧碱性燃料电池中,若正极消耗22.4L气体(标准状况),则转移电子数为2NA | |
| C. | 16.0 gCuO和Cu2S的混合物含阴离子数为0.2NA | |
| D. | 2.24L(标准状况)一氯甲烷分子中含共价键数为0.4NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Na2SiO3水溶液俗称水玻璃,是制备硅胶和木材防火剂的原料 | |
| B. | 为防止食品氧化,常在食品袋中放入装有CaO的透气小袋 | |
| C. | 油脂在人体内水解为氨基酸和甘油等小分子被吸收 | |
| D. | 生产有机玻璃的主要原料为纯碱、石英和石灰石 |
查看答案和解析>>
科目: 来源: 题型:选择题
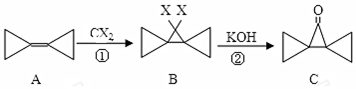
| A. | 反应①是加成反应 | B. | A的所有原子都在一个平面内 | ||
| C. | 反应②是消去反应 | D. | A的二氯代物只有2种 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Y4X10分子中,极性键和非极性键的个数比为10:4 | |
| B. | Z和W形成的多种化合物中只有一种能与水反应 | |
| C. | 25℃时,Z、W、X按原子个数比2:3:4形成的化合物的水溶液的pH=7 | |
| D. | 25℃时,等浓度的Z和Q的最高价氧化物对应水化物的水溶液中,水电离的c(H+)相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com