
科目: 来源: 题型:选择题
| ①常温下,配制0.10moI/L NaHCO3溶液,测其pH为8.4; ②取少量该溶液于试管中,向其中滴加CaCl2溶液至中性,滴加过程中只产生一种白色沉淀(能与盐酸作用产生气体),但无气体放出. |
| A. | NaHCO3溶液呈碱性的原因是HCO3-的水解程度大于电离程度 | |
| B. | 加入CaCl2促进了HCO3-的水解 | |
| C. | 反应的离子方程式是2HCO3-+Ca2+═CaCO3↓+H2CO3 | |
| D. | 反应后的溶液中存在:c(Na+)+2c(Ca2+)═c(HCO3-)+2c(CO32-)+c(Cl-)、 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 制氢弹用到的D、T互为同位素 | |
| B. | 苛性钠溶液可用于治疗胃酸过多 | |
| C. | 硅胶可防止月饼等食品氧化变质 | |
| D. | 向海水中加入净水剂明矾可以使海水淡化 |
查看答案和解析>>
科目: 来源: 题型:解答题
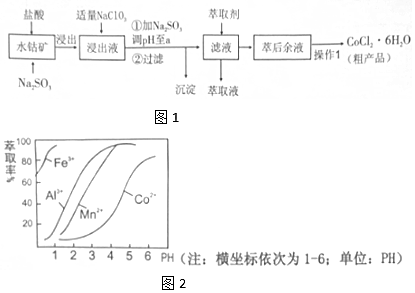
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
查看答案和解析>>
科目: 来源: 题型:解答题
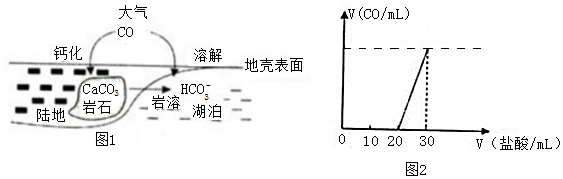
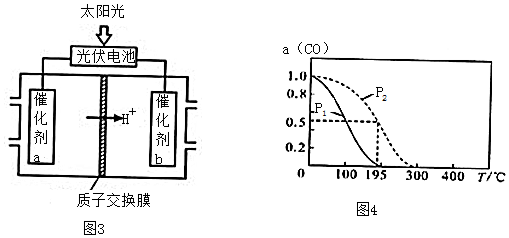
查看答案和解析>>
科目: 来源: 题型:解答题
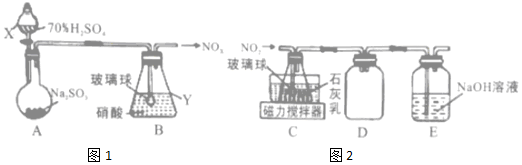
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 二甲苯和四甲苯均有三种 | |
| B. | C3H8和C5H12一定互为同系物 | |
| C. | 石油裂解和油脂皂化均是由高分子物质生成小分子物质的过程 | |
| D. | 乙醇的酯化反应和酯的水解均属于取代反应 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 100g 98%的浓硫酸中含有的氢原子数目为2NA | |
| B. | 16g16O2和18O2的混合物中含有的质子数目为8NA | |
| C. | 电解精炼铜的过程中,若阳极减重64g,则电路中一定通过2NA个电子 | |
| D. | 取50ml14.0mol/L浓硝酸与足量的铜片反应,生成气体分子的数目可能为0.25NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 实验操作 | 实验目的 |
| A | 将C2H4和SO2的混合气体通入足量酸性KmnO4试液中 | 得到纯净的C2H4 |
| B | 向5mL 0.1mol•L-1AgNO3溶液中加1mL0.1mol•L-1NH3•H2O | 制备银氨溶液 |
| C | 向含少量FeBr2的FeCl2溶液中滴入适量新制氯水,并加入CCl4萃取分液 | 制备纯净的FeCl2溶液 |
| D | 向NaCl饱和溶液中先通入NH3至饱和,再通入足量CO2,过滤并洗涤 | 制备NaHCO3固体 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A | B | C | D |
 |  | 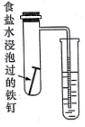 | 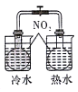 |
| 完成化学能转化为电能 | 证明非金属性强弱 S>C>Si | 验证铁发生析氢腐蚀 | 验证温度对平衡移动的影响 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| 实验操作 | 实验现象 | 结论 | |
| A | 将SO2通人溴水中 | 溴水颜色褪去 | SO2具有漂白性 |
| B | 将铁屑放入稀HNO3中 | 放出无色气体 | Fe比H2活泼 |
| C | 将澄清石灰水滴入某溶液 | 生成白色沉淀 | 溶液中存CO32- |
| D | 将乙烯通入KMnO4酸性溶液 | KMnO4颜色褪去 | 乙烯具有还原性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com