
科目: 来源: 题型:选择题
| 实验目的 | 操作 | |
| A | 比较水和乙醇中羟基氢的活泼性强弱 | 用金属钠分别与水和乙醇反应 |
| B | 欲证明CH2=CHCHO中含有碳碳双键 | 滴入KMnO4酸性溶液,看紫红色是否褪去 |
| C | 检验溴乙烷中的溴原子 | 将溴乙烷与氢氧化钠水溶液共热一段时间,再向冷却后的混合液中滴加硝酸银溶液 |
| D | 制备溴苯 | 苯、溴水和铁屑混合于带长导管的烧瓶中 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 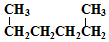 1,4-二甲基丁烷 1,4-二甲基丁烷 | B. | 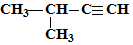 2-甲基-3-丁炔 2-甲基-3-丁炔 | ||
| C. |  2-丁醇 2-丁醇 | D. | CH2Cl-CH2Cl 二氯乙烷 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 饱和纯碱(Na2CO3)溶液中:2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) | |
| B. | 1mol/L的(NH4)2SO4溶液中:c(NH4+)>c(SO42-)>c(H+)>c(OH-) | |
| C. | 0.10mol/L小苏打溶液中:c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-) | |
| D. | 等体积,pH=3的盐酸和醋酸分别与足量锌反应后,c(Cl-)=c(CH3COO-) |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
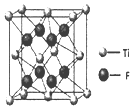 光解水的催化材料可用硝酸镍、硫脲和锐钛矿为原料,采用醇热法制得.
光解水的催化材料可用硝酸镍、硫脲和锐钛矿为原料,采用醇热法制得.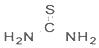 )中C原子轨道的杂化类型为.1mol硫脲中含有σ键的数目为7mol.
)中C原子轨道的杂化类型为.1mol硫脲中含有σ键的数目为7mol.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 常温下$\frac{{K}_{W}}{c({H}^{+})}$=1×10-13mol•L-1的溶液中:Ca2+、Fe2+、NO3-、NH4+ | |
| B. | 水电离出的c (H+)=10-10 mol•L-1的溶液中Na+、K+、Cl?、HCO3? | |
| C. | pH=11的溶液中:CO32-、Na+、AlO2-、NO3-、S2-、SO32- | |
| D. | c(Fe3+)=0.1mol•L-1的溶液中:K+、Cl-、SO42-、H2O2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com