
科目: 来源: 题型:实验题
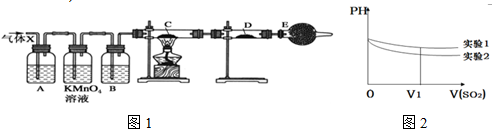
| 实验步骤 | 实验现象 | 结论 |
| 实验1:在盛有不含O2的25ml0.1mol/LBaCl2溶液的烧杯中,缓慢通入纯净的SO2气体 | 假设一成立 | |
| 实验2:在盛有不含O2的25ml0.1mol/LBa(NO3)2溶液的烧杯中,缓慢通入纯净的SO2气体 |
 2NO+4H++3SO42-;.
2NO+4H++3SO42-;.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Ba(NO3)2溶液$\stackrel{通入SO_{2}}{→}$白色沉淀 | |
| B. | 无色溶液$\stackrel{稀HNO_{3}}{→}$ $\stackrel{BaCl_{2}溶液}{→}$白色沉淀 | |
| C. | Ba(NO3)2溶液$\stackrel{加过量HCl}{→}$无现象 $\stackrel{Na_{2}SO_{4}}{→}$白色沉淀 | |
| D. | Fe(NO3)2溶液$\stackrel{加过量HCl}{→}$ $\stackrel{通入SO_{2}}{→}$ $\stackrel{BaCl_{2}}{→}$白色沉淀 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 将1molCl2通入水中,HClO、Cl-、ClO-粒子数之和为2NA | |
| B. | 12gNaHSO4固体中含阳离子数为0.1NA | |
| C. | 标准状况下,22.4LBr2中所含分子数为NA | |
| D. | 7.8gNa2O2与足量的水反应转移电子数为0.2NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 实验 | 现象 | 结论 |
| A | 常温下将Cu放入浓H2SO4中 | 生成刺激性气味气体 | Cu与浓H2SO4反应生成SO2 |
| B | 向某溶液中加入CCl4,振荡后静置 | 液体分层,下层呈紫红色 | 该溶液中存在I- |
| C | 向1.0mol•L-1的NaHCO3溶液中滴加2滴甲基橙 | 溶液呈黄色 | NaHCO3溶液呈碱性 |
| D | 向浓度均为0.1mol•L-1的Al2(SO4)3、Fe2(SO4)3的溶液中逐滴加入氨水 | 先有红褐色沉淀生成,后有白色沉淀生成 | Al(OH)3 的溶度积比Fe(OH)3的大 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:填空题
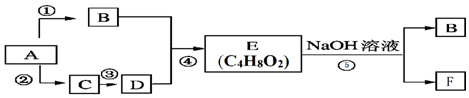

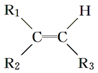 $\stackrel{氧化}{→}$
$\stackrel{氧化}{→}$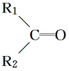 +R3COOH
+R3COOH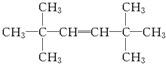 G:
G: .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Mg 为电池的正极 | |
| B. | 负极反应为 AgCl+e-=Ag+Cl- | |
| C. | 可用于海上应急照明供电 | |
| D. | 电池工作时,电解质溶液质量不断减轻 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 无色中性溶液中:Na+、K+、CO32-、SO42- | |
| B. | 含有大量Fe3+的溶液中:Na+、Mg2+、NO3-、I- | |
| C. | 加入铝粉后有气体放出的溶液:Fe2+、K+、NO3-、Cl- | |
| D. | 能使酚酞变红色的溶液:CO32-、Cl-、F-、K+ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 加热能杀死流感病毒是因为蛋白质受热变性 | |
| B. | 用乙醚从黄花蒿中提取青蒿素是利用了氧化还原反应原理 | |
| C. | “丹砂(HgS)烧之成水银,积变又成丹砂.”这个过程是可逆反应 | |
| D. | 丁达尔效应可用于区别溶液与胶体,云、雾、稀硫酸均能产生丁达尔效应 |
查看答案和解析>>
科目: 来源: 题型:解答题

| 沉淀物 | Fe(OH)3 | Al(OH)3 | Co(OH)2 | Fe(OH)2 | Mn(OH)2 |
| 完全沉淀的pH | 3.7 | 5.2 | 9.2 | 9.6 | 9.8 |
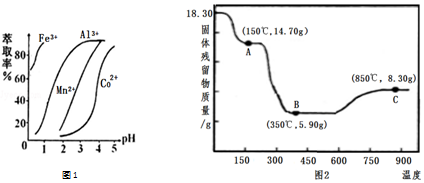
查看答案和解析>>
科目: 来源: 题型:解答题
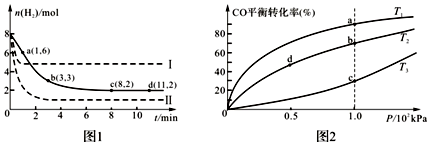
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com