
科目: 来源: 题型:选择题
| A. | 高压钠灯能发出透雾能力强的淡紫色光,常用做路灯 | |
| B. | 用水清洗盛装过浓硫酸的铁捅要远离火源 | |
| C. | 理电池应用广泛,是因为锉能直接与水反应,不需要特殊的电解质溶液 | |
| D. | 据报导,一定条件下氢气可转变为金属氢,金属氢具备超导等优良性能.由氢气转变为金属氢属于同一元索的同位素之间的转化 |
查看答案和解析>>
科目: 来源: 题型:解答题
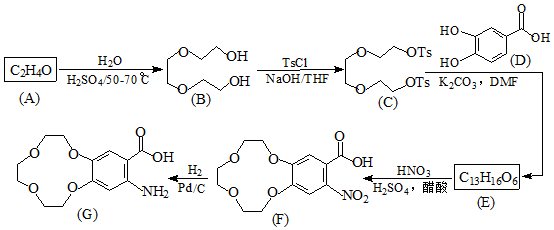
 .
. .
. .
.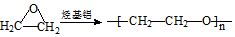 .
.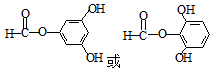 .
.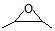 )和邻二苯酚为原料(其它试剂任选),设计制备
)和邻二苯酚为原料(其它试剂任选),设计制备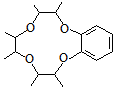 的合成路线.
的合成路线.查看答案和解析>>
科目: 来源: 题型:选择题
 某化学小组拟设计微生物燃料电池将污水中的乙二胺[H2N(CH2)2NH2]氧化成环境友好的物质,工作原理如图所示(a、b均为石墨电极).下列分析正确的是( )
某化学小组拟设计微生物燃料电池将污水中的乙二胺[H2N(CH2)2NH2]氧化成环境友好的物质,工作原理如图所示(a、b均为石墨电极).下列分析正确的是( )| A. | 电子流动方向为a→导线→b | |
| B. | H+经质子交换膜由右向左移动 | |
| C. | 放电一段是时间b极附近pH不变 | |
| D. | a 电极发生反应为:H2N(CH2)2NH2+16e-+4H2O═2CO2↑+N2↑+16H+ |
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 操作 | 现象 | 解释或理论 |
| A | 把铁片投入浓硫酸 | 无明显变化 | 常温下铁不与浓硫酸反应 |
| B | 将浓硫酸滴到白纸上 | 白纸变黑 | 浓硫酸具有强氧化性,导致纸中的纤维素碳化 |
| C | 把二氧化硫通入溴水 | 溴水褪色 | 说明二氧化硫具有漂白性 |
| D | 用湿润的红色石蕊试纸检验某气体 | 试纸变蓝 | 该气体是氨气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
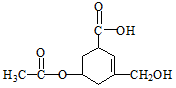
| A. | R的所有原子一定在同一平面上 | |
| B. | 在Ni催化和加热条件下,lmolR能与3molH2发生加成反应 | |
| C. | R既能与羧酸、醇反应,还能发生水解、加成和氧化反应 | |
| D. | 1molR与足量碳酸氢钠溶液反应,生成CO2的物质的量为2mol |
查看答案和解析>>
科目: 来源: 题型:解答题
 铁、铝、铜都是日常生活中常见的金属,它们的单质及其化合物在科学研究和工农业生产中具有广泛用途.请回答以下问题:
铁、铝、铜都是日常生活中常见的金属,它们的单质及其化合物在科学研究和工农业生产中具有广泛用途.请回答以下问题: ;NH4CuSO3中N、S、O三种元素的第一电离能由大到小的顺序为N>O>S(元素符号表示).
;NH4CuSO3中N、S、O三种元素的第一电离能由大到小的顺序为N>O>S(元素符号表示).查看答案和解析>>
科目: 来源: 题型:选择题
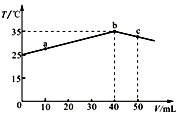
| A. | a→b的过程中,溶液中c(A-)与c(HA)之和始终不变 | |
| B. | c点表示酸碱恰好完全反应 | |
| C. | 等浓度的NaOH和NaA混合溶液中一定存在关系:c(Na+)>c(A-)>c(OH-)>c(H+) | |
| D. | 25℃时,HA的电离平衡常数Ka约为1.43×10-3 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 鉴别苯与四氯化碳:碘水 | |
| B. | 鉴别甲烷与乙烯:酸性高锰酸钾溶液 | |
| C. | 鉴别 与CH≡CH:溴水 与CH≡CH:溴水 | |
| D. | 鉴别NaCl与CH3CH2Cl:硝酸银溶液 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 实验事实 | 结论 | |
| A | 将燃烧的镁条放入CO2中能继续燃烧 | 还原性:Mg>C |
| B | Cl2的水溶液可以导电 | Cl2是电解质 |
| C | 将CO2气体通入苯酚钠溶液出现浑浊 | 酸性:H2CO3>苯酚 |
| D | 某无色溶液中加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝 | 该溶液一定有NH4+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com