
科目: 来源: 题型:实验题
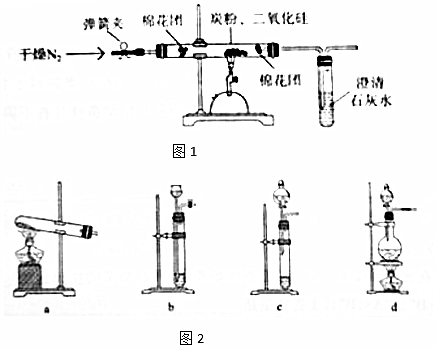
查看答案和解析>>
科目: 来源: 题型:解答题
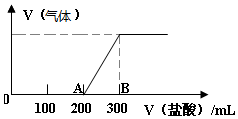 向100mL1.5mol/L的丙溶液中缓慢通入一定量的CO2,充分反应后,向所得溶液中逐滴缓慢滴加0.5mol/L的盐酸,所得气体的体积与所加盐酸的体积(不考虑气体溶解于水)关系如图所示.
向100mL1.5mol/L的丙溶液中缓慢通入一定量的CO2,充分反应后,向所得溶液中逐滴缓慢滴加0.5mol/L的盐酸,所得气体的体积与所加盐酸的体积(不考虑气体溶解于水)关系如图所示.查看答案和解析>>
科目: 来源: 题型:解答题
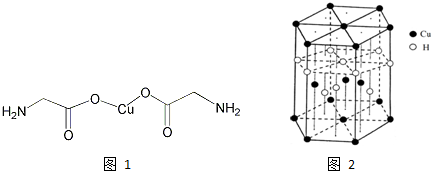
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 将浓硝酸加入盛有铂、金的烧杯中,不反应,再加入一定量浓盐酸后,铂、金溶解,不能说明浓硝酸氧化性比浓盐酸强 | |
| B. | 石英玻璃、普通玻璃、陶瓷及水泥均属于硅酸盐产品 | |
| C. | 电解AlCl3水溶液,阴极周围出现白色胶状沉淀,说明Al(OH)3胶体粒子带正电荷 | |
| D. | 气体甲通入溶液乙,溶液乙的颜色褪去,说明气体甲具有漂白性 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | CaO | B. | Na2CO3 | C. | SiO2 | D. | CaCO3 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:实验题
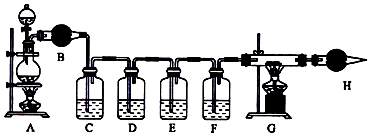
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 采取低碳、节俭的生活方式 | B. | 按规定对生活废弃物进行分类放置 | ||
| C. | 经常使用一次性筷子、塑料袋 | D. | 深入农村和社区,加强环保宣传 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com