
科目: 来源: 题型:选择题
| A. | 依据丁达尔现象可将分散系分为溶液、胶体与浊液 | |
| B. | 直径介于1-100nm之间的微粒称为胶体 | |
| C. | 胶体粒子很小,可以透过半透膜 | |
| D. | 鸡蛋清和豆浆都属于胶体 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 2Na+2H2O═2NaOH+H2↑ | B. | 2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2 | ||
| C. | CuO+CO$\frac{\underline{\;高温\;}}{\;}$Cu+CO2 | D. | Fe+2FeCl3═3FeCl2 |
查看答案和解析>>
科目: 来源: 题型:解答题
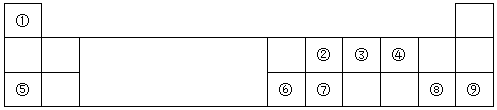
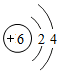 .
.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | O |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑫ | ⑬ |
查看答案和解析>>
科目: 来源: 题型:实验题
| 实验 序号 | t/min C/mol•L-1 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 |
| 1 | 500 | 2.0 | 1.6 | 1.3 | 1.0 | 0.8 | 0.8 |
| 2 | 500 | C2 | 1.2 | 0.8 | 0.8 | 0.8 | 0.8 |
| 3 | 500 | C3 | 1.7 | 1.3 | 1.0 | 1.0 | 1.0 |
| 4 | 600 | 2.0 | 1.1 | 0.9 | 0.9 | 0.9 | 0.9 |
查看答案和解析>>
科目: 来源: 题型:多选题
| 反应时间/min | n(CO)/mol | n(H2)/mol |
| 0 | 0.60 | 1.20 |
| 20 | 0.20 | |
| 30 | 0.40 |
| A. | 反应在20 min内的平均速率为v(H2)=0.04 mol•L-1•min-1 | |
| B. | 保持其他条件不变,升高温度,平衡时c(CH3OH)=0.15 mol•L-1,则反应的△H<0 | |
| C. | 保持其他条件不变,再向平衡体系中同时通入0.20 mol CO、0.20 mol H2、0.20 mol CH3OH,达到新平衡前v(正)>v(逆) | |
| D. | 相同温度下,若起始时向容器中充入1.0 mol CH3OH,达到平衡时CH3OH转化率大于$\frac{1}{3}$ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 该溶液中最多存在4种离子 | |
| B. | 该溶液可由KCl、(NH4)2SO4和FeCl3配制而成 | |
| C. | 该溶液中一定存在Cl-、且c(Cl-)≥0.4mol•L-1 | |
| D. | 该溶液中不能确定是否存在CO32- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | △H1<0 | B. | △H2>0 | C. | △H1=△H3-2△H2 | D. | 2△H4>△H5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com