
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2NO2=N2O4ÓėN2O4=2NO2 | |
| B£® | H2+I2$\frac{\underline{\;\;”÷\;\;}}{\;}$2HIÓė2HI$\frac{\underline{\;\;”÷\;\;}}{\;}$H2+I2 | |
| C£® | CO2+H2O=H2CO3Óė H2CO3=CO2”ü+H2O | |
| D£® | CaO+CO2=CaCO3ÓėCaCO3$\frac{\underline{\;øßĪĀ\;}}{\;}$CaO+CO2”ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ČĪŅāĪ»ÖĆŃ°ÕŅ | B£® | Ļ”ÓŠĘųĢåŌŖĖŲÖŠŃ°ÕŅ | ||
| C£® | ½šŹōŗĶ·Ē½šŹōµÄ·Ö½ēĻß“¦Ń°ÕŅ | D£® | »īĘĆ½šŹōŗĶ»īĘĆ·Ē½šŹōĒųÖŠŃ°ÕŅ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CO2 | B£® | CH4 | C£® | C2H4 | D£® | NH4Cl |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
| A | B | ||
| D | E | G | J |
| L | M | Q |
 £®Š“³öŅ»øöÄܱķŹ¾ŌŖĖŲG”¢J·Ē½šŹōŠŌĒæČõ¹ŲĻµµÄ»Æѧ·½³ĢŹ½H2S+Cl2=2HCl+S”ż»ņNa2S+Cl2=2NaCl+S”ż£®
£®Š“³öŅ»øöÄܱķŹ¾ŌŖĖŲG”¢J·Ē½šŹōŠŌĒæČõ¹ŲĻµµÄ»Æѧ·½³ĢŹ½H2S+Cl2=2HCl+S”ż»ņNa2S+Cl2=2NaCl+S”ż£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | $\frac{mY-XY+2m}{m}$ | B£® | Y-X+2 | C£® | $\frac{mY+XY-2m}{m}$ | D£® | Y-X-2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
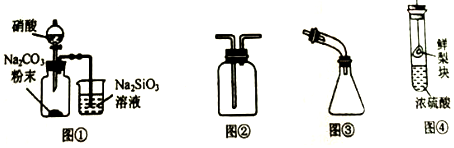
| A£® | Ķ¼¢Ł£ŗÖ¤Ć÷·Ē½šŹōŠŌÓÉĒæµ½ČõµÄĖ³ŠņŹĒN£¾C£¾Si | |
| B£® | Ķ¼¢Ś£ŗŹÕ¼ÆNO2»ņNH3 | |
| C£® | Ķ¼¢Ū£ŗŗ£Ė®ÕōĮóŹ±½ÓŹÕÕōĮóĖ® | |
| D£® | Ķ¼¢Ü£ŗĢ½¾æÅØĮņĖįµÄĶŃĖ®ŠŌ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±ź×¼×“æöĻĀ£¬2.24 LCCl4ÖŠŗ¬ClŌ×ÓŹżÄæĪŖ0.4NA | |
| B£® | 28g¾ŪŅŅĻ©ÖŠĖłŗ¬Ō×ÓŹżĪŖ6NA | |
| C£® | 0.1mol±½ŅŅĻ©ÖŠŗ¬ÓŠĖ«¼üµÄŹżÄæĪŖ0.4NA | |
| D£® | ³£ĪĀ³£Ń¹ĻĀ£¬10 g 46%¾Ę¾«Ė®ČÜŅŗÖŠŗ¬ŃõŌ×Ó×ÜŹżĪŖ0.1NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±ź×¼×“æöĻĀ£¬4.48 LÖŲĖ®£ØD2O£©ÖŠŗ¬ÓŠµÄÖŠ×ÓŹżĪŖ2NA | |
| B£® | 0.1molŅŅĻ©ŗĶŅŅ“¼£ØC2H5OH£¬ÕōĘū£©»ģŗĻĪļĶźČ«Č¼ÉÕĖłĻūŗĵÄŃõ·Ö×ÓŹżŅ»¶ØĪŖ0.3NA | |
| C£® | ³£ĪĀ³£Ń¹ĻĀ£¬15gŅŅĶé·Ö×ÓÖŠŗ¬ÓŠµÄ¹²¼Ū¼üŹżÄæĪŖ3NA | |
| D£® | 273K£¬101kPaĻĀ£¬14gŅŅĻ©Óė±ūĻ©»ģŗĻĪļÖŠŗ¬ÓŠĢ¼Ō×ÓŹżÄæĪŖ3NA |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com