
科目: 来源: 题型:选择题
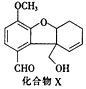
| A. | 分子中含2个手性碳原子 | |
| B. | 分子中所有碳原子均处于同一平面 | |
| C. | 能发生银镜反应,不能发生酯化反应 | |
| D. | 1molX最多能与4molH2发生加成反应 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 液氨气化吸热,可用作制冷剂 | B. | 明矾易溶于水,可用作净水剂 | ||
| C. | 盐酸具有还原性,可用于除去铁锈 | D. | 浓硝酸其有酸性,可用于钝化铁、铝 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 自然界中不存在游离态的碳 | B. | 碳的化合物数量众多,分布极广 | ||
| C. | 向空气中排放二氧化碳会形成酸雨 | D. | 煤、石油、天然气属于可再生碳资源 |
查看答案和解析>>
科目: 来源: 题型:解答题
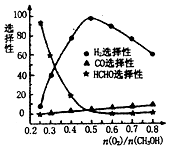 碳元素及其化合物与人类的生活、生产息息相关,请回答下列问题:
碳元素及其化合物与人类的生活、生产息息相关,请回答下列问题:查看答案和解析>>
科目: 来源: 题型:选择题
 LiOH和钴氧化物可用于制备锂离子电池正极材料.利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液.下列说法不正确的是( )
LiOH和钴氧化物可用于制备锂离子电池正极材料.利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液.下列说法不正确的是( )| A. | B极区电解液为LiOH溶液 | |
| B. | 每产生标准状况下2.24L氢气,就有0.1 mol阳离子通过交换膜进入阴极区 | |
| C. | 电解过程中Li+向B电极迁移 | |
| D. | 阳极电极反应式为2Cl--2e-=Cl2↑ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 常温常压下,56g由N2和CO组成的混合气体含有的原子数目为4 NA | |
| B. | 高温下,0.2 molFe与足量水蒸气反应,生成的H2分子数为0.3NA | |
| C. | 1 L 1.0mol•L-1的NaAlO2水溶液中含有的总原子数为2NA | |
| D. | 1 mol羟基中含有的电子数为10NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 实验及现象 | 结论 |
| A | 向AgNO3和AgCl的浊液中滴入0.1mol/LNa2S溶液,生成黑色沉淀 | Ag2S的溶度积比AgCl的小 |
| B | 将光亮镁条放入盛有NH4Cl溶液的试管中,产生大量气泡,同时将湿润的红色石蕊试纸靠近试管口,试纸变蓝 | 反应产生的气体一定是NH3 |
| C | 向溶液X中先滴加稀硝酸,在滴加Ba(NO3)2溶液,出现白色沉淀 | 溶液X中一定含有SO42- |
| D | 将铜粉加入1.0mol/L Fe2(SO4)3溶液中,溶液变蓝 | 说明氧化性Fe3+>Cu2+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:解答题
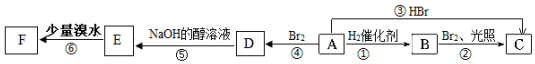
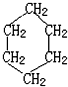 (结构简式).
(结构简式).查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 6种 | B. | 5种 | C. | 4种 | D. | 3种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com