
科目: 来源:2016-2017学年重庆市高二上半期考试化学卷(解析版) 题型:选择题
下列叙述正确的是
A.稀醋酸中加入少量醋酸钠能增大醋酸的电离程度
B.25℃时,在等体积、等浓度的硝酸中加入 氨水,溶液的导电性增强
氨水,溶液的导电性增强
C.25℃时,0.1mol/L的硫化氢溶液与等浓度的硫化钠溶液的导电能力相当
D.25℃时,将等体积pH=1的盐酸和水混合,混合后溶液的pH=1.3
查看答案和解析>>
科目: 来源:2016-2017学年重庆市高二上半期考试化学卷(解析版) 题型:选择题
恒容容器中,2SO2(g) + O2(g) 2SO3 (g) △H=-296.6kJ/mol,下列判断不正确的是
2SO3 (g) △H=-296.6kJ/mol,下列判断不正确的是
A.2体积SO2和足量O2反应,一定不能生成2体积SO3
B.其他条件不变,增大压强,正反应速率增大逆反应速率也增大
C.加入2molSO2和1molO2放出的热量是加入1molSO2和0.5molO2放出热量的2倍
D.平衡后再加入1molSO3,SO2的转化率增大
查看答案和解析>>
科目: 来源:2016-2017学年重庆市高二上半期考试化学卷(解析版) 题型:选择题
右图中的曲线表示在一定条件下,2NO + O2 2NO2 △H<0,反应中NO的转化率与温度的关系。图中标出a、b、c、 d四点,其中表示未达到平衡状态,且v(正)<v(逆)的点是
2NO2 △H<0,反应中NO的转化率与温度的关系。图中标出a、b、c、 d四点,其中表示未达到平衡状态,且v(正)<v(逆)的点是
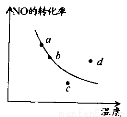
A.a点 B.b点 C.c点 D.d点
查看答案和解析>>
科目: 来源:2016-2017学年重庆市高二上半期考试化学卷(解析版) 题型:选择题
已知某可逆反应在密闭容器中进行:A(g) + 2B(g) 3C(g) + D(s) △H>0,A的转化率与时间t关系如图所示,图中曲线a代表一定条件下该反应的过程。若使a曲线变为b曲线,可能采取的措施是
3C(g) + D(s) △H>0,A的转化率与时间t关系如图所示,图中曲线a代表一定条件下该反应的过程。若使a曲线变为b曲线,可能采取的措施是
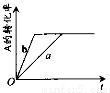
A.增大A的浓度或减少C的浓度
B.缩小容器的容积或加入催化剂
C.升高温度或增大压强
D.由a变成b,A和B的物质的量与C、D的物质的量相等
查看答案和解析>>
科目: 来源:2016-2017学年重庆市高二上半期考试化学卷(解析版) 题型:选择题
在一定温度下,向a L密闭容器中加入1 mol X气体和2mol Y气体,发生如下反应:X(g) + 2Y(g) 2Z(g) △H<0,平衡时生成1.5mol Z。下列说法不正确的是
2Z(g) △H<0,平衡时生成1.5mol Z。下列说法不正确的是
A.增大压强或降低温度,平衡常数K都增大
B.其它条件相同,向容器中只加入2molZ,能建立完全相同的平衡状态
C.平衡时,平衡常数K=36a (mol/L)-1
D.某时刻X、Y、Z物质的量分别是0.3mol,1mol和1.1mol,反应正向进行
查看答案和解析>>
科目: 来源:2016-2017学年重庆市高二上半期考试化学卷(解析版) 题型:选择题
1mol X气体跟a mol Y气体在体积可变的密闭容器中发生如下反应:X(g) + aY(g) bZ(g),反应达到平衡后,测得X的转化
bZ(g),反应达到平衡后,测得X的转化 率为50% 。而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的3/4,则a和b的数值可能是
率为50% 。而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的3/4,则a和b的数值可能是
A.a=l,b=2 B.a=2,b=1 C.a=2,b=2 D.a=3,b=2
查看答案和解析>>
科目: 来源:2016-2017学年重庆市高二上半期考试化学卷(解析版) 题型:选择题
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如下图,下列表述中正确的是
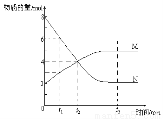
A.反应的化学方程式为: N == 2M
B.t2时,反应物和生成物的浓度相等,达到平衡
C.当M、N都是气体时增大压强,N物质的量减少
D.升高温度,平衡常数K增大,则反应的△H<0
查看答案和解析>>
科目: 来源:2016-2017学年重庆市高二上半期考试化学卷(解析版) 题型:选择题
已知反应mX(g)+nY(g) qZ(g) △H<0,m+n>q,在恒容密闭容器中反应达到平衡时,下列说法不正确的是
qZ(g) △H<0,m+n>q,在恒容密闭容器中反应达到平衡时,下列说法不正确的是
A.通入稀有气体使压强增大,平衡不移动
B.增大压强同时又升高温度,反应速率加快且可以提高Z的产率
C.降低温度,混合气体的平均相对分子质量变大
D.增加X的物质的量,Y的转化率增大
查看答案和解析>>
科目: 来源:2016-2017学年重庆市高二上半期考试化学卷(解析版) 题型:选择题
某温度下CH3COOH和 NH3·H2O的电离常数相等,现向10 mL浓度为0.1 mol·L-1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中
NH3·H2O的电离常数相等,现向10 mL浓度为0.1 mol·L-1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中
A.水的电离程度始终增大
B.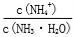 先增大再减小
先增大再减小
C.c(CH3COOH)与c(CH3COO-)之和始终保持不变
D.当加入氨水的体积为10 mL时,c(NH)=c(CH3COO-)
查看答案和解析>>
科目: 来源:2016-2017学年重庆市高二上半期考试化学卷(解析版) 题型:选择题
在一定温度下,将气体X和气体Y各1.6 mol充入10 L恒容密闭容器中,发生反应:X(g)+Y(g) 2Z(g) ΔH。反应过程中测定的数据如下表:
2Z(g) ΔH。反应过程中测定的数据如下表:
t/min | 0 | 2 | 4 | 6 | 8 | … | 16 | 18 |
n(X)/mol | 1.600 | 1.200 | 1.100 | 1.075 | … | … | 1.000 | 1.000 |
下列说法不正确的是
A.4—6 min时间段内Z的平均反应速率2.5×10-3 mol/(L·min)
B.该温度下此反应的平衡常数K=1.44
C.达平衡后,升高温度,K减小,则正反应△H>0
D.其他条件不变,再充入1.6 mol Z,达新平衡时Z的体积分数不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com