
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | C2H5OH£Øl£©+3O2£Øg£©ØT2CO2£Øg£©+3H2O£Øg£©”÷H=-1367.0kJ/mol£ØČ¼ÉÕČČ£© | |
| B£® | H2SO4£Øaq£©+2NaOH £Øaq£©ØTNa2SO4£Øaq£©+2H2O £Øl£©”÷H=-114.6kJ/mol£ØÖŠŗĶČČ£© | |
| C£® | S £Øs£©+O2£Øg£©ØTSO2 £Øg£©”÷H=-296.8kJ/mol£ØČ¼ÉÕČČ£© | |
| D£® | 2NO2ØTO2+2NO”÷H=+116.2kJ/mol£Ø·“Ó¦ČČ£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 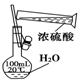 Ļ”ŹĶÅØĮņĖį | B£® | 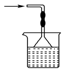 ĪüŹÕ°±Ęų | C£® | 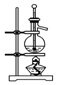 ŹÆÓĶµÄ·ÖĮó | D£® | 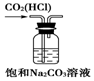 ³żČ„CO2ÖŠµÄHCl |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
 £¬DµÄ¼ņµ„ĘųĢ¬Ēā»ÆĪļµÄæռ乹ŠĶĪŖČż½Ē׶ŠĪ£®
£¬DµÄ¼ņµ„ĘųĢ¬Ēā»ÆĪļµÄæռ乹ŠĶĪŖČż½Ē׶ŠĪ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
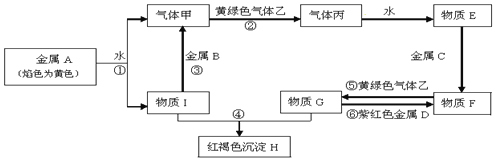
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
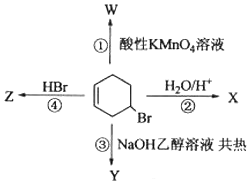
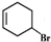 +NaOH$”ś_{”÷}^{“¼}$
+NaOH$”ś_{”÷}^{“¼}$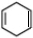 +NaBr+H2O
+NaBr+H2O²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | n£ØCl2£©£ŗn£ØFe£©=5£ŗ4 5Cl2+4Fe$\frac{\underline{\;µćČ¼\;}}{\;}$2FeCl2+2FeCl3 | |
| B£® | n£ØCl2£©£ŗn£ØFeBr2£©=1£ŗ1 Fe2++2Br-+Cl2=Fe3++Br2+2Cl- | |
| C£® | n£ØMnO4-£©£ŗn£ØH2O2£©=2£ŗ3 2MnO4-+3H2O2+6H+=2Mn2++4O2”ü+6H2O | |
| D£® | n£ØFe£©£ŗn[HNO3£ØĻ”£©]=1£ŗ3 4Fe+12H++3NO3-ØT3Fe2++Fe3++3NO”ü+6H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com