
科目: 来源: 题型:选择题
| A. | 在标准状况下,VL气态烯烃(CnH2n)含碳碳双键的数目为$\frac{V}{22.4}$ NA | |
| B. | 在8.4 g NaHCO3晶体中,所含离子数目为0.3NA | |
| C. | 5.6g铁粉与稀硝酸反应,转移的电子数是0.3 NA | |
| D. | 在沸水中滴加含0.1 molFe3+的FeCl3饱和溶液,得到的Fe(OH)3胶粒数为0.1NA |
查看答案和解析>>
科目: 来源: 题型:解答题
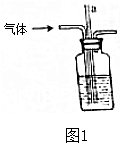 某实验小组设计如下流程,模拟将汽车尾气中的氮氧化物(主要为NO和NO2的混合物)转化为工业用盐亚硝酸钠(NaNO2),并对亚硝酸钠进行多角度探究:汽车尾气$→_{操作①}^{20%NaOH}$溶液$\stackrel{操作②}{→}$固体$→_{③}^{操作}$NaNO2
某实验小组设计如下流程,模拟将汽车尾气中的氮氧化物(主要为NO和NO2的混合物)转化为工业用盐亚硝酸钠(NaNO2),并对亚硝酸钠进行多角度探究:汽车尾气$→_{操作①}^{20%NaOH}$溶液$\stackrel{操作②}{→}$固体$→_{③}^{操作}$NaNO2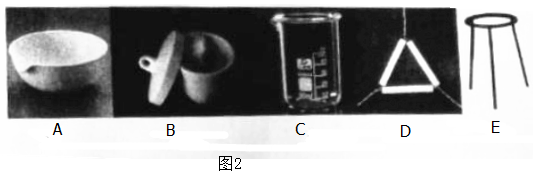
查看答案和解析>>
科目: 来源: 题型:解答题
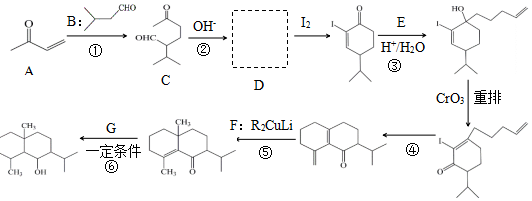
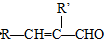 +H2O
+H2O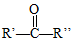 →
→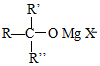 $\stackrel{H+/H_{2}O}{→}$
$\stackrel{H+/H_{2}O}{→}$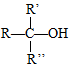

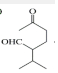 $\stackrel{O{H}^{-}}{→}$
$\stackrel{O{H}^{-}}{→}$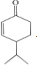 +H2O.
+H2O.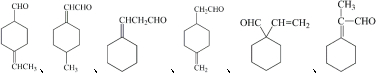
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 1mol 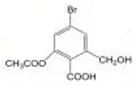 分别与足量的Na、NaOH溶液、NaHCO3溶液反应,最多消耗这三种物质的物质的量分别是2mol、5mol、1mol 分别与足量的Na、NaOH溶液、NaHCO3溶液反应,最多消耗这三种物质的物质的量分别是2mol、5mol、1mol | |
| B. | CH3COOCH2CH3与CH3CH2COOCH3互为同分异构体,1H-NMR谱显示两者均有三种不同的氢原子且三种氢原子的比例相同,故不能用1H-NMR来鉴别 | |
| C. | 乳酸薄荷醇酯(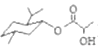 )仅能发生水解、氧化、消去反应 )仅能发生水解、氧化、消去反应 | |
| D. | 与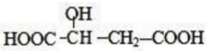 具有官能团种类及数目相同的同分异构体有2种 具有官能团种类及数目相同的同分异构体有2种 |
查看答案和解析>>
科目: 来源: 题型:解答题

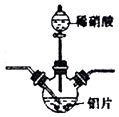
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | a<7 | |
| B. | 该溶液中水电离的c(OH-)=10-amol/L | |
| C. | CH3COO-水解的百分率为$\frac{10-a}{0.1}$×100% | |
| D. | c(CH3COOH)=(l0a-14-10-a)mol/L |
查看答案和解析>>
科目: 来源: 题型:选择题
| W | X | |||
| Y | Z |
| A. | 氢化物沸点:W<Z | B. | 氧化物对应水化物的酸性:Y>W | ||
| C. | 化合物熔点:Y2X3<YZ3 | D. | 简单离子的半径:Y<X |
查看答案和解析>>
科目: 来源: 题型:选择题
| 目的 | 操作 | |
| A. | 取20.00 mL盐酸 | 在50 mL酸式滴定管中装入盐酸,调整初始读数为30.00mL后,将剩余盐酸放入锥形瓶 |
| B. | 清洗碘升华实验所用试管 | 先用酒精清洗,再用水清洗 |
| C. | 测定醋酸钠溶液pH | 用玻璃棒蘸取溶液,点在湿润的pH试纸上 |
| D. | 配制浓度为0.010 mol•L的KMnO4溶液 | 称取KMnO4固体0.158 g,放入100 mL容量瓶中,加水溶解并稀释至刻度 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 植物油氢化过程中发生了加成反应 | |
| B. | 淀粉和纤维素互为同分异构体 | |
| C. | 环己烷与苯可用酸性KMnO4溶液鉴别 | |
| D. | 水可以用来分离溴苯和苯的混合物 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | X的简单氢化物的热稳定性比W强 | |
| B. | Y的简单离子与X的具有相同的电子层结构 | |
| C. | Y与Z形成的化合物的水溶液可使蓝色石蕊试纸变红 | |
| D. | Z与X属于同一主族,与Y属于同一周期 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com