
科目: 来源: 题型:选择题
 改变0.1mol•L-1二元弱酸H2A溶液的pH,溶液中的H2A、HA-、A2-的物质的量分数δ(x)随pH的变化如图所示[已知δ(x)=$\frac{c(X)}{c({H}_{2}A)+c(H{A}^{-})+c({A}^{2-})}$].下列叙述错误的是( )
改变0.1mol•L-1二元弱酸H2A溶液的pH,溶液中的H2A、HA-、A2-的物质的量分数δ(x)随pH的变化如图所示[已知δ(x)=$\frac{c(X)}{c({H}_{2}A)+c(H{A}^{-})+c({A}^{2-})}$].下列叙述错误的是( )| A. | pH=1.2时,c(H2A)=c(HA-) | B. | lg[K2(H2A)]=-4.2 | ||
| C. | PH=2.7时,c(HA-)>c(H2A)=c(A2-) | D. | pH=4.2时,c(HA-)=c(A2-)=c(H+) |
查看答案和解析>>
科目: 来源: 题型:选择题
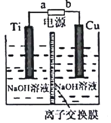
| A. | 待加工铝质工件为阳极 | |
| B. | 可选用不锈钢网作为阴极 | |
| C. | 阴极的电极反应式为:Al3++3e-═Al | |
| D. | 硫酸根离子在电解过程中向阳极移动 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 糖类化合物也可称为碳水化合物 | |
| B. | 维生素D可促进人体对钙的吸收 | |
| C. | 蛋白质是仅由碳、氢、氧元素组成的物质 | |
| D. | 硒是人体必需的微量元素,但不宜摄入过多 |
查看答案和解析>>
科目: 来源: 题型:解答题
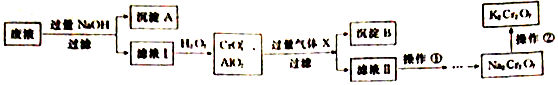
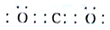 (填电子式)
(填电子式)查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 标准状况下,足量Fe与22.4 L Cl2反应,转移的电子数为2NA | |
| B. | 0.1molO2完全反应时,转移的电子数一定为 0.4 NA | |
| C. | 用惰性电极电解CuSO4溶液后,如果加入0.1mol Cu(OH)2能使溶液复原,则电路中转移电子的数目为 0.2NA | |
| D. | 常温常压下,100 g 17% H2O2水溶液中含氧原子总数为NA |
查看答案和解析>>
科目: 来源: 题型:选择题
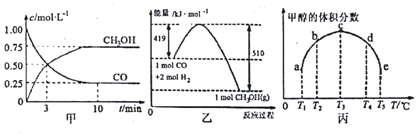
| A. | 若改为加入A物质可加快反应速率 | |
| B. | 达新平衡后B的转化率减小,A的转化率增大 | |
| C. | 达新平衡后A与B的转化率均增大 | |
| D. | 达新平衡后B的转化率不变,A的转化率增大 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 60g丙醇中含有的共价键的数目为10NA | |
| B. | 在含有1molFeI2 的溶液中,通过足量的氯气,转移的电子数是3NA | |
| C. | 某溶液中Na2CO3和NaHCO3的浓度均为0.1mol/L,Na+离子总数为0.3NA | |
| D. | 50mL 12mol/L 盐酸与足量MnO2共热,转移的电子数为0.3NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 为了防止富脂食品氧化变质,延长食品的保质期,常在包装袋中放入生石灰 | |
| B. | 海水中含有丰富的碘元素,因此碘被称为“海洋元素” | |
| C. | 工业生产玻璃、水泥、漂白粉,均需要用石灰石为原料 | |
| D. | 可以利用氯化铁溶液的酸性清除铜镜表面的铜锈 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com