
科目: 来源: 题型:选择题
| A. | Fe2O3+3CO═2Fe+3CO2△H=-24.8 kJ•mol-1(反应热) | |
| B. | CH3OH(g)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g)△H=-192.9 kJ•mol-1(反应热) | |
| C. | C4H10(g)+$\frac{13}{2}$O2(g)═4CO2(g)+5H2O(g)△H=-2 658.0 kJ•mol-1(燃烧热) | |
| D. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=+57.3 kJ•mol-1(中和热) |
查看答案和解析>>
科目: 来源: 题型:填空题
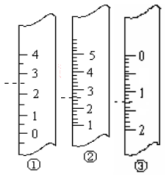 (1)如图分别是温度计、量筒、滴定管的一部分,则:温度计应该是①,读数是2.5℃,量筒应该是②,读数为2.5 mL,滴定管应该是③,读数为1.30 mL
(1)如图分别是温度计、量筒、滴定管的一部分,则:温度计应该是①,读数是2.5℃,量筒应该是②,读数为2.5 mL,滴定管应该是③,读数为1.30 mL查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①④ | B. | ①④ | C. | ②④ | D. | ①③ |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
 (1)利用N2和H2可以实现NH3的工业和成,而氨又可以进一步制备硝酸.已知:
(1)利用N2和H2可以实现NH3的工业和成,而氨又可以进一步制备硝酸.已知:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 清洗仪器时,判断洗涤干净的标准是器壁内出现均匀水膜,既不聚成水滴,也不成股流下 | |
| B. | 从滴瓶中取用试剂时,滴管的尖嘴可以接触试管内壁 | |
| C. | 滴定接近终点时,滴定管的尖嘴可以接触锥形瓶内壁 | |
| D. | 向容量瓶转移液体时,引流用玻璃棒可以接触容量瓶内壁 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com