
科目: 来源: 题型:选择题
| A. | 加热NH4Cl只破坏离子键 | |
| B. | N2H4中极性键与非极性键的比值是1:4 | |
| C. | PCl3和BCl3分子中所有原子的最外层都达到8电子稳定结构 | |
| D. | 某元素最高价氧化物的水化物和氢化物的化学式分别为H2XO4、H2X |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | X和Y形成的化合物中一定不含共价键 | |
| B. | W的氧化物的水化物是强酸 | |
| C. | ZX2能使酸性KMnO4溶液褪色,说明ZX2具有漂白性 | |
| D. | X和Z的简单氢化物沸点差异大,主要原因是氢键的影响 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 淀粉、纤维素不能互称同分异构体 | |
| B. | 油脂在碱性条件下的水解反应成为皂化反应 | |
| C. | 向鸡蛋清溶液中加入NaCl(s)时,因蛋白质变性致溶液变浑浊 | |
| D. | 使用酸性K2Cr2O7检验酒驾的过程中,乙醇表现还原性 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 该化合物仅含碳、氢两种元素 | B. | 该化合物中碳、氢原子个数比为1:6 | ||
| C. | 无法确定该化合物是否含有氧元素 | D. | 该化合物中一定含有氧元素 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 操作及预期现象 | 结论 | |
| A | 向25mL冷水和沸水中分别滴入5滴FeCl3饱和溶液,前者为黄色,后者为红褐色 | 温度升高,Fe3+的水解程度增大 |
| B | 向某无色溶液滴加硝酸酸化的BaCl2溶液,产生白色沉淀 | 原溶液中一定含有SO42- |
| C | A1箔插入稀HNO3中,无现象 | A1箔表面被HNO3氧化,形成致密的氧化膜 |
| D | 用洁净铂丝蘸取溶液进行焰色反应,火焰呈黄色 | 原溶液中有Na+无K+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:解答题
 利用氨气脱硝(除NO)是大气污染防治研究的热点,脱硝过程中涉及的反应为:
利用氨气脱硝(除NO)是大气污染防治研究的热点,脱硝过程中涉及的反应为:查看答案和解析>>
科目: 来源: 题型:选择题
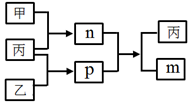 短周期主族元素A、B、C、D的原子序数依次增大,C和D位于同一主族.m、n、p均为由这些元素组成的二元化合物,甲、乙、丙为其中三种元素对应的单质,丙为淡黄色固体,易溶在BD2中,p的水溶液是一种二元弱酸,有漂白性.上述物质的转化关系如图所示(反应条件省略).下列说法正确的是( )
短周期主族元素A、B、C、D的原子序数依次增大,C和D位于同一主族.m、n、p均为由这些元素组成的二元化合物,甲、乙、丙为其中三种元素对应的单质,丙为淡黄色固体,易溶在BD2中,p的水溶液是一种二元弱酸,有漂白性.上述物质的转化关系如图所示(反应条件省略).下列说法正确的是( )| A. | 原子半径:A<B<C | |
| B. | BD2分子中所有原子都达到了8电子稳定结构 | |
| C. | C与D的简单氢化物沸点,后者高 | |
| D. | 非金属性:D>C>B |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 异丁烷的所有原子都位于同一平面上 | |
| B. | 苯和溴水反应制取溴苯属于加成反应 | |
| C. | 糖类在酸性条件下水解产物均为葡糖糖 | |
| D. | 乙基环己烷的一溴代物有6种 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | c、d、e最高价氧化物水化物的酸性e>d>c | |
| B. | b氢化物的沸点比e氢化物的沸点高 | |
| C. | a的氧化物和c的氧化物都具有两性 | |
| D. | e的氧化物通入Ba(NO3)2溶液中有沉淀产生 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 以苯为萃取剂萃取溴水中的溴,分液时应从下口放出苯溶液 | |
| B. | 蒸馏过程时,加热一段时间后,忘加沸石,应停止加热立刻补加 | |
| C. | 分离I2和铁粉的混合物,可加热,利用I2易升华的特性分离 | |
| D. | 配置1mol/L的盐酸,定容后摇匀,液面下降,不影响准确性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com