
科目: 来源: 题型:选择题
| A. | 常温下,1 L 0.1 mol/L的NH4NO3溶液中氢原子总数为0.4NA | |
| B. | 0.5 mol 甲基中电子数为5NA | |
| C. | 在反应3Br2+3CO32-=5Br-+BrO3-+3CO2↑中,每生成3 mol CO2转移的电子数为5NA | |
| D. | 常温常压下,22.4 L N2H4中N-H键数为4NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Na | B. | Mg | C. | Al | D. | Fe |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:实验题

查看答案和解析>>
科目: 来源: 题型:实验题
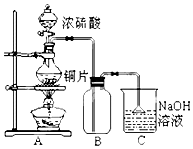 某研究性学习小组的同学为验证浓硫酸与铜能反应而稀硫酸不能,设计了如图所示装置进行探究:将6.4g 铜片和含0.2moL溶质的18.4mol/L浓硫酸放在圆底烧瓶中共热,直到无气体生成为止.(假定在此过程溶液体积不变)
某研究性学习小组的同学为验证浓硫酸与铜能反应而稀硫酸不能,设计了如图所示装置进行探究:将6.4g 铜片和含0.2moL溶质的18.4mol/L浓硫酸放在圆底烧瓶中共热,直到无气体生成为止.(假定在此过程溶液体积不变)| 序号 | 不合理的原因 | 误差 (偏低或偏高) | 改变措施 |
| 方案① | |||
| 方案② |
查看答案和解析>>
科目: 来源: 题型:实验题

查看答案和解析>>
科目: 来源: 题型:选择题
| 溶质 | NaF | NaClO | NaHCO3 | Na2CO3 |
| pH | 7.5 | 9.7 | 8.2 | 11.6 |
| A. | pH=2的HF溶液与pH=12的NaOH溶液以体积比1:1混合,则有:c(Na+)>c(F-)>c(OH-)>c(H+) | |
| B. | 加热0.1 mol•L-1 NaClO溶液测其pH,pH大于9.7 | |
| C. | 0.1 mol•L-1 Na2CO3溶液中,存在关系:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3) | |
| D. | 电离平衡常数大小关系:K(HF)>K(H2CO3 )>K(HClO)>K( HCO3-) |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | $\frac{n}{98}$moL | B. | $\frac{7n}{98}$moL | C. | $\frac{4n}{98}$moL | D. | $\frac{4n}{32}$moL |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 升高温度,正向反应速率增加,逆向反应速率减小 | |
| B. | 压缩容器体积平衡向正反应方向移动,达到新的平衡后c(A2)变小 | |
| C. | 平衡后加入A2,达到新的平衡A2 和B2的转化率均增大 | |
| D. | 达到平衡后,降低温度或增大压强都有利于该反应平衡正向移动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com