
科目: 来源: 题型:选择题
| A. | 醋酸溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO-) | |
| B. | 10mL0.01mol•L-1的CH3COOH溶液中加水稀释,溶液中c(OH-)减小 | |
| C. | 向醋酸溶液中加少量的CH3COONa固体,平衡逆向移动 | |
| D. | 常温下pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合后,溶液的pH<7 |
查看答案和解析>>
科目: 来源: 题型:解答题
 为探究乙烯与溴的加成反应,甲同学设计并进行如下实验:先用乙醇和浓硫酸为原料制取乙烯(CH3CH2OH$→_{170℃}^{浓硫酸}$ CH2═CH2↑+H2O),将生成的气体直接通入溴水中,发现溴水褪色,即证明乙烯与溴水发生了加成反应.乙同学发现在甲同学的实验中,产生的气体有刺激性气味,推测在制得的乙烯中还可能含有少量有还原性的杂质气体,由此他提出必须先把杂质气体除去,再与溴水反应.
为探究乙烯与溴的加成反应,甲同学设计并进行如下实验:先用乙醇和浓硫酸为原料制取乙烯(CH3CH2OH$→_{170℃}^{浓硫酸}$ CH2═CH2↑+H2O),将生成的气体直接通入溴水中,发现溴水褪色,即证明乙烯与溴水发生了加成反应.乙同学发现在甲同学的实验中,产生的气体有刺激性气味,推测在制得的乙烯中还可能含有少量有还原性的杂质气体,由此他提出必须先把杂质气体除去,再与溴水反应.查看答案和解析>>
科目: 来源: 题型:实验题
 .
.查看答案和解析>>
科目: 来源: 题型:解答题
| 沸点/℃ | 溶解性 | 与饱和NaHSO3溶液混合 | |
| A | 75.7 | 微溶于水 | 发生化合反应,生成沉淀 |
| B | 118 | 溶于水 | 不反应 |
| C | 34 | 微溶于水,与B互溶 | 不反应 |

查看答案和解析>>
科目: 来源: 题型:选择题
| A. | PM2.5亦称可入肺颗粒物,表面积相对较大,会吸附有害物质 | |
| B. | 煤的气化和石油的分馏都是物理变化 | |
| C. | 从海水中提取物质都必须通过化学反应才能实现 | |
| D. | “嫦娥”三号使用的碳纤维是一种新型的有机高分子材料 |
查看答案和解析>>
科目: 来源: 题型:解答题
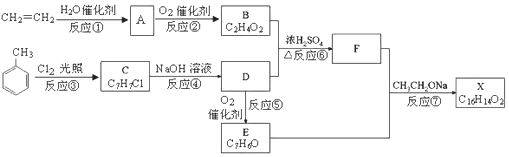
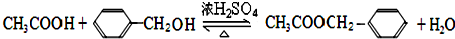 .
.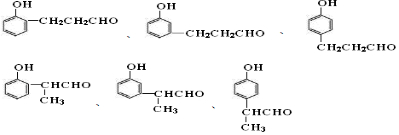 中的任意一种.
中的任意一种.查看答案和解析>>
科目: 来源: 题型:解答题


查看答案和解析>>
科目: 来源: 题型:实验题
| 序号 | 条件 | 现象 | 结论 | |
| 温度/℃ | 催化剂 | |||
| 1 | 40 | FeCl3溶液 | ||
| 2 | 20 | FeCl3溶液 | ||
| 3 | 20 | MnO2 | ||
| 4 | 20 | 无 | ||


查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 异戊二烯与等物质的量的Br2发生反应 | |
| B. | 2-氯丁烷与NaOH乙醇溶液共热发生反应 | |
| C. | 丙烯与H2O在催化剂作用下发生反应 | |
| D. | 新戊烷和氯气生成一氯代物的反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com