
科目: 来源: 题型:解答题
 尿素[CO(NH2)2]是首个由无机物人工合成的有机物.
尿素[CO(NH2)2]是首个由无机物人工合成的有机物.查看答案和解析>>
科目: 来源: 题型:推断题

查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题

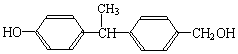 b.
b.
 d.
d.
 结构相似的醇不能被氧化为醛或酸.
结构相似的醇不能被氧化为醛或酸.
 .
.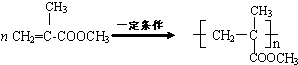 .
.查看答案和解析>>
科目: 来源: 题型:推断题

 .
. .
.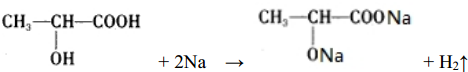 .
. .
. .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 金属钠与氧气反应,条件不同产物不同 | |
| B. | 金属钠着火可用水扑灭 | |
| C. | 少量的钠可保存在汽油里 | |
| D. | 钠的化学性质活泼,可从硫酸铜溶液中置换出铜 |
查看答案和解析>>
科目: 来源: 题型:实验题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 向饱和碳酸钠溶液中通入二氧化碳:CO32-+CO2+H2O═2HCO3- | |
| B. | 二氧化锰与浓盐酸反应:MnO2+4HCl(浓)═Mn2++2Cl2↑+2H2O | |
| C. | 亚硫酸氢钠溶液中加过量澄清石灰水:2HSO3-+Ca2++2OH-═CaSO3↓+2H2O+SO32- | |
| D. | 金属钠与硫酸铜溶液反应:2Na+2H2O+Cu2+$\frac{\underline{\;\;△\;\;}}{\;}$2Na++Cu(OH)2↓+H2↑ |
查看答案和解析>>
科目: 来源: 题型:解答题
 元素X、Y、Z为前四周期元素,X的基态原子核外电子有21种运动状态,元素Y的原子最外层电子数是其内层的3倍,Z与X、Y不在同一周期,且Z原子核外p电子比s电子多5个.
元素X、Y、Z为前四周期元素,X的基态原子核外电子有21种运动状态,元素Y的原子最外层电子数是其内层的3倍,Z与X、Y不在同一周期,且Z原子核外p电子比s电子多5个. )裂化生成苯和丙烯.
)裂化生成苯和丙烯.查看答案和解析>>
科目: 来源: 题型:实验题
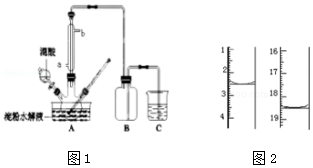
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com