
科目: 来源: 题型:实验题

查看答案和解析>>
科目: 来源: 题型:解答题
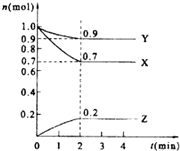 某温度时.在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示.
某温度时.在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示.查看答案和解析>>
科目: 来源: 题型:推断题
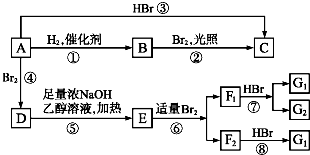
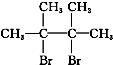 ,F1和F2、G1和G2分别互为同分异构体.
,F1和F2、G1和G2分别互为同分异构体.查看答案和解析>>
科目: 来源: 题型:解答题
 实验室制备1,2-二溴乙烷的反应原理如下:
实验室制备1,2-二溴乙烷的反应原理如下:| 乙醇 | 1,2-二溴乙烷 | 乙醚 | 液溴 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 | 红色发烟液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 | 3.12 |
| 沸点/℃ | 78.5 | 132 | 34.6 | 58.8 |
| 熔点/℃ | -l30 | 9 | -1l6 | -7.2 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
 五种前四周期元素X、Y、Z、W、R在元素周期表中的位置如图所示.下列有关元素的叙述中,正确的是( )
五种前四周期元素X、Y、Z、W、R在元素周期表中的位置如图所示.下列有关元素的叙述中,正确的是( )| A. | W的简单氢化物的沸点比X的简单氢化物的沸点低 | |
| B. | 五种元素均在元素周期表的s区 | |
| C. | 电负性和第一电离能均为:Y>X>W | |
| D. | 五种元素的单质中Z的单质的沸点最高 |
查看答案和解析>>
科目: 来源: 题型:选择题
 已知:下表为25℃时某些弱酸的电离平衡常数.
已知:下表为25℃时某些弱酸的电离平衡常数.| CH3COOH | HClO | H2CO3 |
| Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.4×10-7Ka2=4.7×10-11 |
| A. | 25℃时,相同浓度的CH3COONa溶液的碱性大于NaClO溶液 | |
| B. | 向NaClO溶液中通入少量二氧化碳的离子方程式为:2ClO-+CO2+H2O═2HClO+CO32- | |
| C. | 导电能力:c>a | |
| D. | 图象中a点酸的总浓度小于b点酸的总浓度 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | HCO3-+H2O?H3O++CO32- | B. | HCO3-+OH-=H2O+CO32- | ||
| C. | HCO3-+H2O?H2CO3+OH- | D. | HCO3-+H3O+=2H2O+CO2↑ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ②③ | B. | ②④ | C. | ①③ | D. | ①④ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 0.2mol/L的硫酸10mL | B. | 0.25mol/L的盐酸20mL | ||
| C. | 18.4mol/L的硫酸30mL | D. | 0.3mol/L的硝酸20mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com