
科目: 来源: 题型:选择题
| A. | 铜元素发生了氧化反应 | B. | 反应中只有O2得电子 | ||
| C. | 32gO2参与反应,转移电子4mol | D. | Cu2S既被氧化又被还原 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ① | B. | ①② | C. | ③④ | D. | ①④ |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
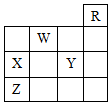
| A. | 五种元素中,只有Z为金属元素 | |
| B. | W位于ⅥA族,有+6、-2两种常见化合价 | |
| C. | X和Y的最高价氧化物对应水化物都是强酸 | |
| D. | X、Y、Z的气态氢化物的稳定性:Y>X>Z |
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | 向Al2(SO4)3溶液中加入过量的NH3•H2O:Al3++4NH3•H2O=AlO2-+4NH4++2H2O | |
| B. | Fe(NO3)2溶液中加入稀硫酸溶液:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O | |
| C. | c(Fe2+ )=1 mol•L-1的溶液中存在:K+、NH4+、MnO4-、SO42- | |
| D. | 如图所示实验可证明元素的非金属性:Cl>C>Si |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 苯和水 | B. | 溴苯和苯 | C. | 食盐水和泥沙 | D. | 硝酸钾和硫酸钠 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 编号 | 电极材料. | 电解质溶液 | 电流计指针 |
| 1 | Mg、Al | 稀盐酸 | 偏转 |
| 2 | Al、Cu | 稀盐酸 | 偏转 |
| 3 | A1、C(石墨) | 稀盐酸 | 偏转 |
| 4 | Mg、Al | 氢氧化钠溶液 | 偏转 |
| 5 | Al、Zn | 浓硝酸 | 偏转 |
| A. | 实验1、2中铝所作的电极(正极或负极)不相同 | |
| B. | 实验2、3中,铝电极的电极反应式均为Al-3e-═Al3+ | |
| C. | 实验4中铝电极的电极反应式为:Al-3e-+40H-═A102-+2H2O | |
| D. | 实验5中铝作原电池的负极 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 78g Na2O2中含有的离子总数为4NA | |
| B. | 标准状况下,1.12L HF中所含的分子总数为0.05NA | |
| C. | 由CO2和O2组成的混合物共有NA个分子,其中的氧原子数为2NA | |
| D. | 0.11mol•L-1 FeCl3溶液中含有的Cl-数目为0.3NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com