
科目: 来源: 题型:解答题
 液氨气化后分解产生的氢气可作为燃料供给氢氧燃料电池.
液氨气化后分解产生的氢气可作为燃料供给氢氧燃料电池.查看答案和解析>>
科目: 来源: 题型:选择题
 在t℃时,Ag2CrO4(橘红色) 在水溶液中沉淀溶解平衡曲线如图所示.又知AgCl的Ksp=1.8×10-10.下列说法正确的是( )
在t℃时,Ag2CrO4(橘红色) 在水溶液中沉淀溶解平衡曲线如图所示.又知AgCl的Ksp=1.8×10-10.下列说法正确的是( )| A. | 将AgNO3溶液滴加到KCl溶液中,反应的活化能几乎为零 | |
| B. | t℃时,Ag2CrO4的Ksp=1×10-8 | |
| C. | 饱和Ag2CrO4溶液中,加入水能使溶液由X点变为Y点 | |
| D. | t℃时,AgCl比Ag2CrO4的溶解度大 |
查看答案和解析>>
科目: 来源: 题型:选择题
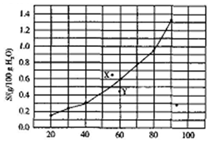
| A. | 溴酸银的溶解是一个熵增、焓减过程 | |
| B. | 对应温度下,X点的分散系中,V(溶解)>v(沉淀) | |
| C. | Y点的分散系中,c(Ag+)•c(BrO3-)>6.25×10-4 | |
| D. | 60℃时溴酸银饱和溶液中c(BrO3-)=0.025mol•L-1 |
查看答案和解析>>
科目: 来源: 题型:选择题
 25℃时,用0.01mol•L-1的氢氧化钠溶液滴定20mL同浓度的HA溶液,滴定曲线如图所示[AG=1g$\frac{c({H}^{+})}{c(O{H}^{-})}$].下列有关叙述正确的是( )
25℃时,用0.01mol•L-1的氢氧化钠溶液滴定20mL同浓度的HA溶液,滴定曲线如图所示[AG=1g$\frac{c({H}^{+})}{c(O{H}^{-})}$].下列有关叙述正确的是( )| A. | 由图可知HA为强酸 | |
| B. | 滴定终点应为于OA段之间 | |
| C. | A点对应溶液中:c(A-)=c(Na+) | |
| D. | 当滴入NaOH溶液10mL时,所得溶液中:c(Na+)>c(A-)>c(HA)>c(H+)>c(OH-) |
查看答案和解析>>
科目: 来源: 题型:实验题
 (1)a图中的图1表示10mL量筒中液面的位置,A与B,B与C刻度间相差1mL,如果刻度A为4,量简中液体的体积是3.2mL.
(1)a图中的图1表示10mL量筒中液面的位置,A与B,B与C刻度间相差1mL,如果刻度A为4,量简中液体的体积是3.2mL.| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 理论解释 | 结论 |
| A | H-N的键能大于H-P | 沸点:NH3>PH3 |
| B | 离子半径:Mg2+<Ba2+ | 热分解温度:碳酸镁髙于碳酸钡 |
| C | 离子半径:Na+<Cs+ | 配位数(C.N.):NaCl<CsCl |
| D | 晶格能:FeS2>ZnS | 岩浆中的硫化物矿物析出顺序ZnS先于FeS2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 向纯水中加入少量固体碳酸钠,c(H+)减小,Kw不变,促进水的电离 | |
| B. | 向纯水中加入稀氨水,平衡逆向移动,c(OH-)增大,变小 | |
| C. | 将纯水加热到95℃时,变大,pH不变,水仍呈中性 | |
| D. | 向水中加入A1C13固体,平衡正向移动,c(OH-)增大 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 化学反应速率变化时,化学平衡一定发生移动 | |
| B. | 化学平衡发生移动时,化学反应速率一定变化 | |
| C. | 正反应进行的程度大,正反应速率一定大 | |
| D. | 化学反应速率变化而化学平衡不移动的情况,只有使用催化剂条件下才会发生 |
查看答案和解析>>
科目: 来源: 题型:实验题
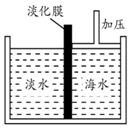 海水中含有丰富的Na+、Mg2+、Cl-、Br-等化学资源.将海水淡化与浓缩海水结合是综合利用海水资源的途径之一.以浓缩海水为原料,通过一系列工艺流程可以提取Mg、Br2等产品.
海水中含有丰富的Na+、Mg2+、Cl-、Br-等化学资源.将海水淡化与浓缩海水结合是综合利用海水资源的途径之一.以浓缩海水为原料,通过一系列工艺流程可以提取Mg、Br2等产品.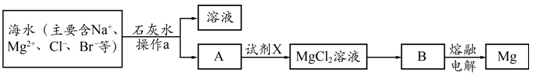
查看答案和解析>>
科目: 来源: 题型:解答题
| 有机物A | 有机物B | 有机物C | 有机物D |
| ①可用于果实催熟 ②比例模型为  | ①由C、H两种元素组成 ②球棍模型为  | ①生活中常见的液态有机物,分子中碳原子数与有机物A相同 ②能与Na反应,但不能与NaOH反应 | ①相对分子质量比有机物C大14 ②能由有机物C氧化生成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com