
科目: 来源: 题型:选择题

| A. | 甲表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为483.6KJ•mol-1 | |
| B. | 乙表示恒温恒容条件下发生的可逆反应2NO2(g)?N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 | |
| C. | 丙表示A、B两物质的溶解度随温度变化情况,将A、B饱和溶液分别由t1℃升温至t2℃时,溶质的质量分数B>A | |
| D. | 丁表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH小于NaB溶液 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 标准状况下,5.6LCO2与足量Na2O2反应转移的电子数为0.5NA | |
| B. | 2.0gH218O与D2O的混合物中所含中子数为NA | |
| C. | 1molFeBr2与足量的氯气反应时转移的电子数为2NA | |
| D. | 25℃时pH=11的Na2CO3溶液中水电离出的OH-的数目为0.001NA |
查看答案和解析>>
科目: 来源: 题型:实验题
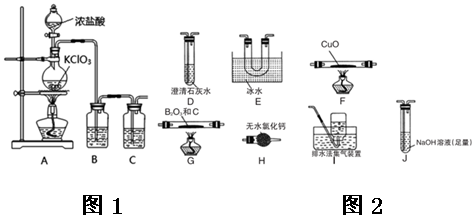
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:选择题
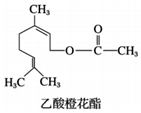 乙酸橙花酯是一种食用香料,其结构简式如图,关于该有机物的叙述中正确的是( )
乙酸橙花酯是一种食用香料,其结构简式如图,关于该有机物的叙述中正确的是( )| A. | ②④⑤ | B. | ①④⑤ | C. | ②③⑥ | D. | ②③④ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 无色溶液中可能大量存在:Al3+、NH4+、Cl-、S2- | |
| B. | 0.1 mol/LFeCl3溶液中大量存在:Fe2+、NH4+、SCN-、SO42- | |
| C. | 加入Al粉产生H2的溶液中可能大量存在:K+、Na+、NO3-、Cl- | |
| D. | 中性溶液中可能大量存在:Fe3+、K+、Cl-、SO42- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 18 gD2O含电子数目为10NA | |
| B. | 1 L 0.1 mol/L NH4NO3溶液中含有氮原子数目为0.2 NA | |
| C. | 0.1 mol CaC2固体含离子数目为0.3 NA | |
| D. | agC2H4和C3H6混合气体含原予数目为aNA/14 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 肯定有SO2和NO | B. | 肯定没有NO2和O2,可能有Cl2 | ||
| C. | 可能有Cl2和O2 | D. | 肯定只有NO |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 该晶体类型是原子晶体 | |
| B. | 晶体中碳原子数与C-O化学键数之比为1:2 | |
| C. | 晶体的空间最小环共有6个原子构成 | |
| D. | 该晶体中碳原子和氧原子的个数比为1:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com