
科目: 来源: 题型:选择题
| A. | 氢氧化铁与盐酸反应:H++OH-═H2O | |
| B. | 铁与盐酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 氧化铜溶于稀硫酸:CuO+2H+═Cu2++H2O | |
| D. | 向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O═Fe(OH)3↓+3H+ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 碱性氧化物:Na2O、CaO、Mn2O7、Na2O2 | |
| B. | 碱:NaOH、KOH、Ba(OH)2、Na2CO3 | |
| C. | 铵盐:NH4Cl、NH4NO3、(NH4)2SO4、NH3•H2O | |
| D. | 氧化物:CO2、NO、SO2、H2O |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 热稳定性:PH3<SiH4<NH3<HF | |
| B. | 微粒直径大小:S2->Cl->Mg2+>Na+ | |
| C. | 酸性强弱:HClO<H2CO3<H2SO3<HBrO4 | |
| D. | 熔点高低:石墨>食盐>干冰>液溴 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 24372.86 kJ | B. | 21.44 kJ | C. | 600.20 kJ | D. | 21435.71 kJ |
查看答案和解析>>
科目: 来源: 题型:选择题
 某气态不饱和链烃CxHy在一定条件下与H2加成为CxHy+m,取CxHy和H2混合气体共120mL进行实验,发现随混合气体中H2所占体积的变化,反应后得到的气体总体积数也不同,反应前混合气体中H2所占的体积V(H2)和反应后气体总体积V(反应后总)的关系如图所示(气体体积均在同温间压下测定)由此可知m的数值为( )
某气态不饱和链烃CxHy在一定条件下与H2加成为CxHy+m,取CxHy和H2混合气体共120mL进行实验,发现随混合气体中H2所占体积的变化,反应后得到的气体总体积数也不同,反应前混合气体中H2所占的体积V(H2)和反应后气体总体积V(反应后总)的关系如图所示(气体体积均在同温间压下测定)由此可知m的数值为( )| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 总质量一定的油脂,无论以何种比例组合,完全水解后生成甘油的量不变 | |
| B. | 用甘氨酸(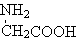 )和丙氨酸( )和丙氨酸( )缩合最多可形成4种二肽 )缩合最多可形成4种二肽 | |
| C. | 用碳酸钠溶液不能区分乙醇、乙酸、苯和硝基苯四种有机物 | |
| D. | 苯酚和苯甲醇互为同系物,均能使酸性高锰酸钾溶液褪色 |
查看答案和解析>>
科目: 来源: 题型:选择题
 对于锌、铜和稀硫酸组成的原电池(如图),下列有关说法正确的是( )
对于锌、铜和稀硫酸组成的原电池(如图),下列有关说法正确的是( )| A. | ①② | B. | ①②③ | C. | ②③④ | D. | ①②③④ |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com