
科目: 来源: 题型:选择题
| A. | 溴水 | B. | NaHCO3溶液 | C. | 乙醇 | D. | 酸性KMnO4溶液 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 元素Y、Z、W具有相同电子层结构的离子,其半径依次增大 | |
| B. | 元素X与元素Y形成的化合物X2Y2中既有极性共价键又有非极性共价键 | |
| C. | 元素Y、R分别与元素X形成的化合物的热稳定性:XmY<XmR | |
| D. | 元素W、R的最高价氧化物的水化物都是强酸 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 用酸性KMnO4溶液鉴别乙烯和CH2=CH-CH3 | |
| B. | 将铁屑、溴水、苯混合制溴苯 | |
| C. | 检验蔗糖是否水解:取1mL 20%的蔗糖溶液,加3~5滴稀硫酸.水浴加热5min后取少量溶液,再加入少量新制备的Cu(OH)2,加热3~5 min,观察实验现象 | |
| D. | 将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 0.8 mol•L-1 | B. | 1.6 mol•L-1 | C. | 1.4 mol•L-1 | D. | 0.75 mol•L-1 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①④⑤ | B. | ①③④ | C. | ③⑤ | D. | ②③ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. |  2,3-二甲基-3-乙基丁烷 2,3-二甲基-3-乙基丁烷 | B. |  2,2,3,-四甲基己烷 2,2,3,-四甲基己烷 | ||
| C. |  对二甲苯 对二甲苯 | D. |  2,4,4-三甲基戊烯 2,4,4-三甲基戊烯 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 用氯酸钾制取氧气时可加入少量的高锰酸钾以加快反应速率 | |
| B. | 为加快制取氢气的速率用锌粉代替锌粒 | |
| C. | 为降低HNO3与Cu反应制备NO2的速率可以采用稀硝酸代替浓硝酸 | |
| D. | 为了延长食品的保质期在食品包装袋中加入硅胶、硫酸亚铁 |
查看答案和解析>>
科目: 来源: 题型:选择题
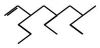 命名正确的是( )
命名正确的是( )| A. | 5,7-二甲基-3-乙基-1-辛烯 | B. | 3-乙基-5,7-二甲基-1-壬烯 | ||
| C. | 3-甲基-5-乙基-7-丙基-8-壬烯 | D. | 7-甲基-5-乙基-3-丙基-1-壬烯 |
查看答案和解析>>
科目: 来源: 题型:解答题


| BaCO3 | BaSO4 | BaSO3 | BaS2O3 |
| 5.1×10-9 | 1.1×10-10 | 8.4×10-7 | 1.6×10-5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com