
科目: 来源: 题型:解答题

| 硫酸% | 31.52 | 36.10 | 40.67 | 45.25 |
| 锰浸出率 | 77.42 | 89.49 | 91.59 | 97.95 |
| 黄铁矿% | 12.5 | 15 | 17.5 | 20 |
| 锰浸出率 | 88.79 | 97.95 | 99.18 | 99.46 |
| A | 硫酸45.25% | B | 硫酸31.52% | C | 硫酸45.25% | D | 硫酸36.10% |
| 黄铁矿20% | 黄铁矿15% | 黄铁矿15% | 黄铁矿20% |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
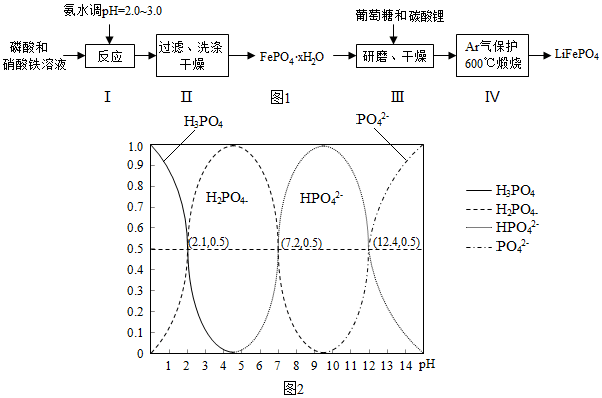
| 实验序号 | 1 | 2 | 3 |
| 固体失重质量分数 | 19.9% | 20.1% | 20.0% |
查看答案和解析>>
科目: 来源: 题型:解答题

| 物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 | HVO3 |
| 溶解性 | 可溶 | 难溶 | 难溶 | 易溶 | 难溶 |

查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 不能判断溶液中是否存在SO42- | B. | 溶液中一定不存在的离子是CO32 | ||
| C. | 不能判断溶液中是否存在Ag+ | D. | 不能判断是否含有[Al(OH)]4-离子 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合:Ba2++2OH-+NH4++HCO3-=BaCO3↓+NH3•H2O+H2O | |
| B. | 实验室配制的亚铁盐溶液在空气中被氧化:4Fe2++O2+2H2O=4Fe3++4OH- | |
| C. | 向碳酸氢铵溶液中加过量石灰水并加热:NH4++OH-$\frac{\underline{\;△\;}}{\;}$NH3↑+H2O | |
| D. | 用酸化的高锰酸钾溶液氧化双氧水:2MnO4-+6H++H2O2═2Mn2++3O2↑+4H2O |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | pH=7的溶液:Fe3+、NH4+、Cl-、NO3- | |
| B. | 水电离出的c(H+)=$\sqrt{{K}_{w}}$的溶液中:Na+、SO42-、CO32-、K+ | |
| C. | 由水电离出的c(OH-)=1.0×10-2 mol•L-1的溶液:Cl-、CH3COO-、K+、[Al(OH)4]- | |
| D. | $\frac{[O{H}^{-}]}{[{H}^{+}]}$=1012的溶液中,NH4+、Al3+、NO3-、Cl- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 放电时Pb为负极,此时溶液中的SO42-向Pb电极迁移 | |
| B. | 铅蓄电池电解CuCl2溶液,若制得2.24LCl2(标准状况),这时电池内消耗的H2SO4至少0.2mol | |
| C. | 放电完全后铅蓄电池可进行充电,此时铅蓄电池的负极连接外电源的正极上 | |
| D. | 充电时阳极的电极反应式:PbSO4+2H2O-2e-=PbO2+4H++SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com