
科目: 来源: 题型:选择题
 下列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
下列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )| a | b | c | |
| A | Al | AlCl3 | Al(OH)3 |
| B | NO | NO2 | HNO3 |
| C | Si | SiO2 | H2SiO3 |
| D | FeS2 | SO2 | H2SO4 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 以石墨为电极电解MgCl2溶液:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$ Cl2+H2↑+2OH- | |
| B. | 泡沫灭火器工作时化学反应:2Al3++3CO32-+6H2O=Al(OH)3↓+3CO2↑ | |
| C. | KI溶液中滴入稀硫酸,空气中振荡:4H++4I-+O2═2I2+2H2O | |
| D. | 向NH4HCO3溶液中加过量的NaOH溶液并加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O |
查看答案和解析>>
科目: 来源: 题型:实验题
 能源与材料、信息被称为现代社会发展的三大支柱,化学与能源有着密切联系.
能源与材料、信息被称为现代社会发展的三大支柱,化学与能源有着密切联系.| 化学键 | H-H | Cl-Cl | H-Cl |
| 键能 | 436 | 243 | 431 |
查看答案和解析>>
科目: 来源: 题型:解答题

 ;
;查看答案和解析>>
科目: 来源: 题型:填空题
 ;C2B2的电子式为
;C2B2的电子式为 .
.查看答案和解析>>
科目: 来源: 题型:实验题
查看答案和解析>>
科目: 来源: 题型:解答题
 将一定量的钠铝合金置于水中,合金全部溶解,得到 20 mL pH=14的溶液,然后用1mol•L-1的盐酸滴定,沉淀质量与消耗盐酸的体积关系如图所示,写出有关反应的化学方程式
将一定量的钠铝合金置于水中,合金全部溶解,得到 20 mL pH=14的溶液,然后用1mol•L-1的盐酸滴定,沉淀质量与消耗盐酸的体积关系如图所示,写出有关反应的化学方程式查看答案和解析>>
科目: 来源: 题型:填空题
 甲酸乙酯,
甲酸乙酯, .
.
查看答案和解析>>
科目: 来源: 题型:解答题
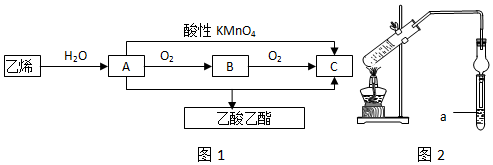
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com