
科目: 来源: 题型:选择题
| A. | 微粒半径:O2-<F-<Na+<Li+ | |
| B. | 单质的熔点:Li<Na<K<Rb | |
| C. | 分子中的键角:CH4>H2O>CO2 | |
| D. | 晶格能由大到小:NaF>NaCl>NaBr>NaI |
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气 | |
| B. | 原混合酸中NO3-物质的量为0.4 mol | |
| C. | 第二份溶液中最终溶质为FeSO4 | |
| D. | 取20 mL原混合酸加水稀释至1 L后溶液c(H+)=0.1mol•L-l |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 反应①的平衡常数K1=$\frac{c(C{O}_{2})•c(Cu)}{c(CO)•c(CuO)}$ | |
| B. | 反应③的平衡常数K=$\frac{{K}_{1}}{{K}_{2}}$ | |
| C. | 对于反应③,恒容时,温度升高,H2浓度减小,则该反应的焓变为正值 | |
| D. | 对于反应③,恒温恒容下,增大压强,H2浓度一定减小 |
查看答案和解析>>
科目: 来源: 题型:解答题
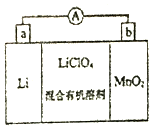 锰锂电池的体积小、性能优良,是常用的一次电池.该电池反应原理如图所示,其中电解质LiClO4溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2.回答下列问题:
锰锂电池的体积小、性能优良,是常用的一次电池.该电池反应原理如图所示,其中电解质LiClO4溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2.回答下列问题:查看答案和解析>>
科目: 来源: 题型:解答题
 .由18O、16O、H、D原子组成的H2O2分子共有9种.
.由18O、16O、H、D原子组成的H2O2分子共有9种.查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:实验题

 ,能证明凯库勒观点错误的实验现象是a烧瓶中产生“喷泉”现象.
,能证明凯库勒观点错误的实验现象是a烧瓶中产生“喷泉”现象. .试回答:
.试回答:查看答案和解析>>
科目: 来源: 题型:选择题
 ).下列有关它的说法不正确的是( )
).下列有关它的说法不正确的是( )| A. | 分子式为C10H16 | B. | 分子中所有碳原子可能共平面 | ||
| C. | 其一氯代物有9种 | D. | 能与溴水发生加成反应 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 乙烷(乙烯):光照条件下通入Cl2,气液分离 | |
| B. | 溴苯(液溴):用氢氧化钠溶液洗涤,分液 | |
| C. | 乙烯(SO2):气体通过盛酸性高锰酸钾溶液的洗气瓶 | |
| D. | 乙醇(水):加足量浓硫酸,蒸馏 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 甲烷与乙烯共lmol,完全燃烧后生成2molH2O | |
| B. | 光照下,异丁烷与Cl2发生取代反应生成的一氯代物有2种 | |
| C. | 乙烯可以用作生产食品包装材料的原料 | |
| D. | 乙酸分子中含有碳氧双键,所以它能使溴水褪色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com