
科目: 来源:2016-2017学年湖南省浏阳市高二上阶段性测试化学试卷 题型:填空题
火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态N2O4。已知①2O2(g)+N2(g)=N2O4(l)ΔH1
②N2(g)+2H2(g)=N2H4(l)ΔH2
③O2(g)+2H2(g)=2H2O(g)ΔH3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g)ΔH4=-1048kJ/mol
(1)上述反应热效应之间的关系式为ΔH4=________________,
(2)又已知H2O(l)=H2O(g)ΔH=+44kJ/mol。则16g液态肼与液态N2O4反应生成液态水时放出的热量是kJ。
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是。
(4)合成氨工业中氢气可由天然气和水反应制备,其主要反应为:CH4(g)+2H2O(g) CO2(g)+4H2(g)已知,破坏1mol化学键需要吸收的热量如下表所示:
CO2(g)+4H2(g)已知,破坏1mol化学键需要吸收的热量如下表所示:
化学键 | C—H | O—H | C=O | H—H |
吸收热量(kJ/mol) | 414 | 464 | 803 | 436 |
试通过计算得出该反应的ΔH=_________kJ/mol,
查看答案和解析>>
科目: 来源:2016-2017学年湖南省浏阳市高二上阶段性测试化学试卷 题型:简答题
(1)CrO42?和Cr2O72?在溶液中可相互转化。室温下,初始浓度为1.0mol·L?1的Na2CrO4溶液中c(Cr2O72?)随c(H+)的变化如下图所示。

①用离子方程式表示Na2CrO4溶液中的转化反应。
②由图可知,溶液酸性增大,CrO42?的平衡转化率__________(填“增大“减小”或“不变”)。
③升高温度,溶液 中CrO42?的平衡转化率减小,则该反应的ΔH_______0(填“大于”“小于”或“等于”)。
中CrO42?的平衡转化率减小,则该反应的ΔH_______0(填“大于”“小于”或“等于”)。
(2)+6价铬的化合物毒性较大,常用NaHSO3将废液中的Cr2O72?还原成Cr3+,反应的离子方程式为。
查看答案和解析>>
科目: 来源:2016-2017学年湖南省浏阳市高二上阶段性测试化学试卷 题型:填空题
A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的气球。关闭K2,将等量且少量的NO2通过K1、K3分别充入A、B中,反应起始时,A、B的体积相同。(已知:2NO2 N2O4
N2O4 )
)
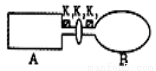
(1)一段时间后,反应达到平衡,此时A、B中生成的N2O4的速率是v(A)________(填“>”、“<”、“=”)v(B);若打开活塞K2,气球B将________(填“增大”、“减小”、“不变”)。
(2)若平衡后在A、B中再充入与初始量相等的NO2,则达到平衡时,A中的NO2转化率________,B中的NO2转化率将________(填“增大”、“减小”、“不变”);若通入等量的Ne气,则达到平衡时,A中的NO2转化率________,B中的NO2转化率将________(填“增大”、“减小”、“不变”)。
(3)室温下,若A、B都保持体积不变,将A套上—个绝热层,B与外界可以进行热传递,则达到平衡时,____________中的颜色较深。
(4)若在容器A中充入4.6g的NO2,达到平衡后容器内混合气体的平均相对分子质量为57.5,则平衡时的N2O4物质的量为_______________。
查看答案和解析>>
科目: 来源:2016-2017学年湖南省浏阳市高二上阶段性测试化学试卷 题型:简答题
反应 (△H<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如下图所示:
(△H<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如下图所示:

回答问题:
⑴反应的化学方程式中a∶b∶c为;
⑵A的平均反应速率vⅠ(A)、vⅡ(A)、vⅢ(A)从大到小排列次序为;
⑶B的平衡转化率αⅠ(B)、αⅡ(B)、αⅢ(B)中最小的是,其值是;
⑷由第一次平衡到第二次平衡,平衡移动的方向是,采取的措施是;
⑸比较第Ⅱ阶段反应温度(T2)和第Ⅲ阶段反应温度(T3)的高低;T2T3(填“<”“>”“=”)判断的理由是。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com