
科目: 来源: 题型:选择题
| A. |  如图所示装置完成实验室制氨气 | |
| B. | 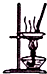 如图所示装置蒸发FeCl3溶液制备无水FeCl3 | |
| C. | 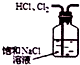 如图所示装置除去HCl中含有的少量Cl2 | |
| D. |  如图所示装置可用于分离二氧化锰和二氯化锰 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | K+、NH4+、HCO3-、AlO2- | B. | K+、Cl-、Fe3+、SO42- | ||
| C. | K+、I-、ClO-、Na+ | D. | Na+、SO32-、S2-、Cl- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 该化合物含有离子键和共价键 | |
| B. | 1molO2参与该反应时,得到1mol电子 | |
| C. | 该化合物中阳离子与阴离子个数比为2:1 | |
| D. | O2PtF6的熔点可能比O2低 |
查看答案和解析>>
科目: 来源: 题型:解答题
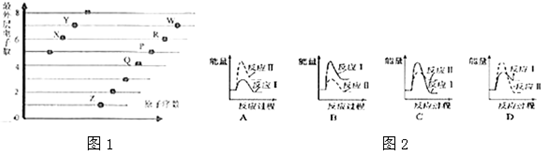
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ⅣA族元素形成的氢化物的沸点从上到下依次递增,则ⅤA族元素所形成的氢化物的沸点从上到下也是依次递增 | |
| B. | 氯气可置换出KEr溶液中的溴,则氟气也可置换出KBr中的溴 | |
| C. | 某浓度的NaClO溶液的pH=d,则其中由水电离出的c(H+)=10-14+dmon•L-1 | |
| D. | 某温度下,MgCO3的Ksp=6.8×10-6,则该温度下所有含固体MgCO3的溶液,都有c(Mg2+)=c(CO32-),且c(Mg2+)•c(CO32-)=6.8×10-6 |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:c(Na+ )=c(NO3 - ) | |
| B. | 1.0 mol•L-1Na2CO3 溶液:c(OH-)=c(HCO3-)+c(H+) | |
| C. | pH=8.0的KHS溶液中,c(K+)>c(HS-)>c(OH-)>c(S2-)>c(H+) | |
| D. | 将0.2 mol•L-1的某一元酸HA溶液和0.1 mol•L-1NaOH溶液等体积混合后,溶液pH大于7,则反应后的混合液中:2c(OH-)+c (A-)=2c(H+)+c(HA) |
查看答案和解析>>
科目: 来源: 题型:选择题
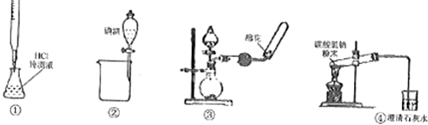
| A. | 利用装置①进行盐酸待测溶液浓度的测定 | |
| B. | 利用装置②分离碘酒中碘和酒精 | |
| C. | 利用装置③制备收集干燥氨气 | |
| D. | 利用装置④加热分解碳酸氢钠 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | FeCl3溶液中:K,CH3OH,Br-,NO3- | |
| B. | 在氨水溶液中:Al3+,NO3-,Cl-,Ag+ | |
| C. | 某透明澄清的溶液中:NH4+,Fe3+,NO3-,Cl- | |
| D. | 能使甲基橙显红色的溶液:K+,Cr2O72-,CH2CH2OH,SO42- |
查看答案和解析>>
科目: 来源: 题型:解答题
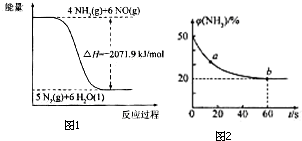 合理应用和处理氮的化合物,在生产生活中有重要意义.
合理应用和处理氮的化合物,在生产生活中有重要意义.查看答案和解析>>
科目: 来源: 题型:选择题
| 序号 | ① | ② | ③ | ④ |
| 溶液 | NaCl | CH4COONH4 | NaF | NaHCO3 |
| pH | 7.0 | 7.0 | 8.1 | 8.4 |
| A. | 酸性强弱:H2CO3>HF | |
| B. | ①和②中溶质均未水解 | |
| C. | 离子的总浓度:①>③ | |
| D. | ④中:c(HCO3-)+2c(CO32-)+c(H2CO3)=0.1mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com