
科目: 来源: 题型:解答题
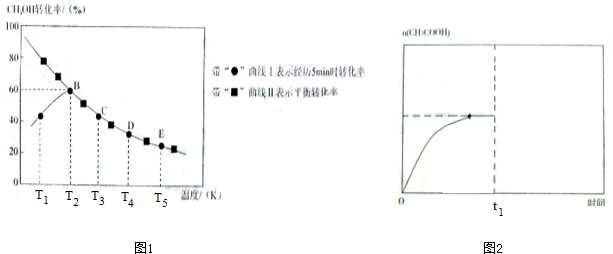
查看答案和解析>>
科目: 来源: 题型:解答题
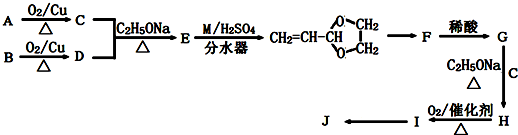
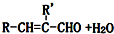

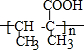 .
.查看答案和解析>>
科目: 来源: 题型:多选题
| A. | X、Y元素能与氢形成分子式为H2XY2、H4X2Y2等弱酸 | |
| B. | 化合物ZY2中只含有离子键 | |
| C. | 工业上可用X单质置换ZY得到Z单质 | |
| D. | Y的氢化物的沸点比其下一周期的同族元素的氢化物的沸点低 |
查看答案和解析>>
科目: 来源: 题型:解答题
 .
.查看答案和解析>>
科目: 来源: 题型:选择题
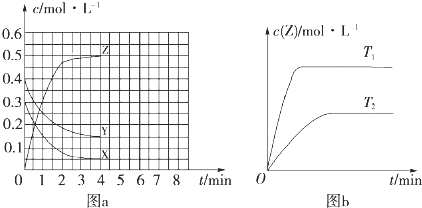
| A. | 发生反应时,各物质的反应速率大小关系为v(X)=v (Y)=2 v (Z) | |
| B. | 图a 中反应达到平衡时,Y 的转化率为37.5% | |
| C. | T0 时,该反应的平衡常数为 33.3 | |
| D. | 该反应正反应的反应热△H<0 |
查看答案和解析>>
科目: 来源: 题型:解答题
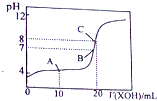 X、Y是元素周期表前20号元素,且X的原子序数比Y大4,请填空(X、Y要用具体的元素符号表示):
X、Y是元素周期表前20号元素,且X的原子序数比Y大4,请填空(X、Y要用具体的元素符号表示):查看答案和解析>>
科目: 来源: 题型:填空题
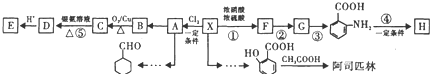
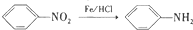 (苯胺、易被氧化)
(苯胺、易被氧化)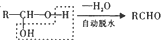
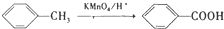
 ;
;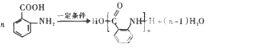 ;
;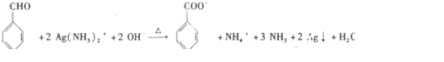 .
.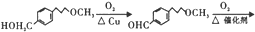 完成
完成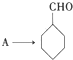 的流程图
的流程图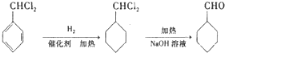 ;
;查看答案和解析>>
科目: 来源: 题型:解答题
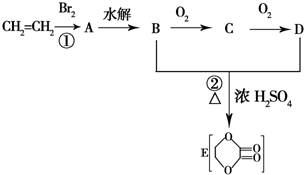 由乙烯和其他无机原料合成环状 化合物其合成过程如图(水及其他无机产物均已省略):
由乙烯和其他无机原料合成环状 化合物其合成过程如图(水及其他无机产物均已省略):查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com