
科目: 来源: 题型:填空题
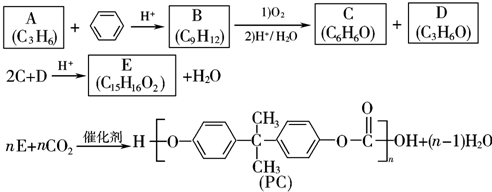
 .
. .
. (写出结构简式).
(写出结构简式).查看答案和解析>>
科目: 来源: 题型:填空题
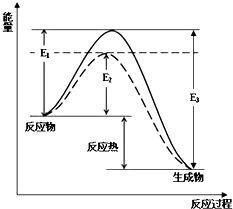 (1)工业合成氨是一个可逆反应:N2(g)+H2(g)?2NH3(g).图中虚线部分是通过改变化学反应中的条件,请解释原因:下表为不同温度下该反应的平衡常数.由此可推知,表中T1<573K(填“>”、“<”或“=”).
(1)工业合成氨是一个可逆反应:N2(g)+H2(g)?2NH3(g).图中虚线部分是通过改变化学反应中的条件,请解释原因:下表为不同温度下该反应的平衡常数.由此可推知,表中T1<573K(填“>”、“<”或“=”). | T/K | T1 | 573 | T3 |
| K | 1.00×107 | 2.54×105 | 1.88×103 |
| pH | <8.0 | 8.0~9.6 | >9.6 |
| 颜色 | 黄色 | 绿色 | 蓝色 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | NaHSO3溶液:c(OH-)=c(HSO3-)+c(H+)+c(H2SO3) | |
| B. | CuSO4•(NH4)2SO4•6H2O的溶液中:c(SO42-)>c(NH4+)>c(Cu2+)>c(H+)>C(OH-) | |
| C. | 氯气溶于水达到平衡后,若其他条件不变加入CaCO3固体,$\frac{c({H}^{+})}{c(HClO)}$增加 | |
| D. | NaSiO3溶液加水稀释后,恢复至原温度,pH和KW均减小 |
查看答案和解析>>
科目: 来源: 题型:填空题
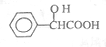 ,工业上扁桃酸可以由烃A经过以下步骤合成得到:
,工业上扁桃酸可以由烃A经过以下步骤合成得到: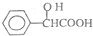
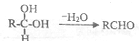
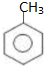 ;扁桃酸中含氧官能团名称羟基、羧基.
;扁桃酸中含氧官能团名称羟基、羧基. .
.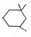 )在浓硫酸作用下反应生成,请写出反应的化学方程式
)在浓硫酸作用下反应生成,请写出反应的化学方程式
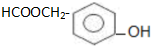 .
.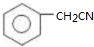 )为原料合成扁桃酸的同分异构体-对羟基苯乙酸(
)为原料合成扁桃酸的同分异构体-对羟基苯乙酸(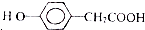 )的合理路线.
)的合理路线.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:选择题
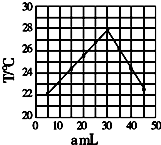 将amL 0.1mol/LHCl溶液和bmL未知浓度的NaOH溶液混合均匀后,测量并记录溶液温度,实验结果如图(实验中始终保持a+b=50ml).下列叙述正确的是( )
将amL 0.1mol/LHCl溶液和bmL未知浓度的NaOH溶液混合均匀后,测量并记录溶液温度,实验结果如图(实验中始终保持a+b=50ml).下列叙述正确的是( )| A. | 做该实验时,环境温度为22摄氏度 | |
| B. | 该实验表明化学能可能转化为热能 | |
| C. | NaOH溶液的浓度约为0.1mol/L | |
| D. | 该实验表明有水生成的反应都是放热反应 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 27gAl与足量浓硫酸混合,产生气体33.6L(标况) | |
| B. | 1molSiO2与C完全反应,生成标准状况气体44.8L | |
| C. | 电解精炼Cu时,阳极每溶解12.8gCu,阴极析出0.2molCu | |
| D. | 1mol/L的某一元酸溶液,测得pH=3,溶液中c(OH-)一定为1×10-11 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 铜与浓硫酸反应所得白色固体甲是CuSO4 | |
| B. | 加BaCl2溶液后所得白色沉淀是BaSO3 | |
| C. | 白色固体甲中夹杂的少量黑色物质乙中不可能含有CuO | |
| D. | 白色固体甲中夹杂的少量黑色物质乙中含元素Cu、S |
查看答案和解析>>
科目: 来源: 题型:解答题
 Ⅰ、试分析比较合成氨与用SO2和O2反应制SO3的反应
Ⅰ、试分析比较合成氨与用SO2和O2反应制SO3的反应查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com