
科目: 来源: 题型:填空题


查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 含有离子键的化合物一定是离子化合物 | |
| B. | 同种非金属元素间不可能形成离子键 | |
| C. | 非金属元素间不可能形成离子化合物 | |
| D. | 分子中一定存在共价键 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 左、下方区域的金属元素 | |
| B. | 右、上方区域的非金属元素 | |
| C. | 金属元素与非金属元素分界线附近的元素 | |
| D. | 过渡元素中 |
查看答案和解析>>
科目: 来源: 题型:解答题
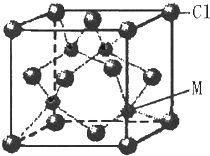 已知W、X、Y、Z、R五种元素是短周期的元素,原子序数依次增大,其中X 的基态原子中成对的电子的对数与单个电子的数目相同,Y 是地壳中含量最多的元素,R的单质是淡黄色固体,不溶于水,能溶于CS2.在短周期中:W的原子半径最小,Z 的原子半径最大.又知M是第四周期的元素,M的最外层只有一个单电子,次外层的轨道上全部填充满了电子.
已知W、X、Y、Z、R五种元素是短周期的元素,原子序数依次增大,其中X 的基态原子中成对的电子的对数与单个电子的数目相同,Y 是地壳中含量最多的元素,R的单质是淡黄色固体,不溶于水,能溶于CS2.在短周期中:W的原子半径最小,Z 的原子半径最大.又知M是第四周期的元素,M的最外层只有一个单电子,次外层的轨道上全部填充满了电子.查看答案和解析>>
科目: 来源: 题型:解答题
 稀土元素是宝贵的战略资源,我国的蕴藏量居世界首位.
稀土元素是宝贵的战略资源,我国的蕴藏量居世界首位.查看答案和解析>>
科目: 来源: 题型:解答题
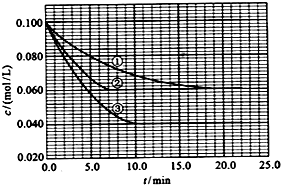
 X、Y、Z三种短周期元素,它们的原子序数之和为16.X、Y、Z三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如下变化:
X、Y、Z三种短周期元素,它们的原子序数之和为16.X、Y、Z三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如下变化:
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Na2O2既是氧化剂又是还原剂 | |
| B. | Na2FeO4既是氧化产物又是还原产物 | |
| C. | 3molNa2O2发生反应,有12mol电子转移 | |
| D. | Na2FeO4在水中被氧化得到Fe3+,Fe3+水解生成氢氧化铁,可净水 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 在100℃、101 kPa条件下,液态水的气化热为40.69 kJ•mol-1,则H2O(g)?H2O(l) 的△H=+40.69 kJ•mol-1 | |||||||||||
| B. | 已知MgCO3的Ksp=6.82×10-6,则所有含有固体MgCO3的溶液中,都有c(Mg2+)=c(CO32-),且c(Mg2+)•c(CO32-)=6.82×10-6 | |||||||||||
| C. | 已知:
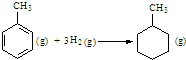 的△H为-384 kJ•mol-1 的△H为-384 kJ•mol-1 | |||||||||||
| D. | 常温下,在0.10 mol•L-1的NH3•H2O溶液中加入少量NH4Cl晶体,能使NH3•H2O的电离度降低,溶液的pH减小 |
查看答案和解析>>
科目: 来源: 题型:选择题
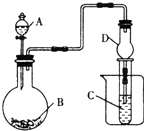
| A. | 若A为浓盐酸,B为KMnO4(KMnO4在常温下能与浓盐酸反应),C中盛品红溶液,则C中溶液褪色 | |
| B. | 若A为硫酸,B为大理石,C中盛澄清石灰水,则C中溶液先出现浑浊后变澄清 | |
| C. | 若A为浓氨水,B为生石灰,C中盛AlCl3溶液,则C中先产生白色沉淀后沉淀溶解 | |
| D. | 上述实验中仪器D可以用长玻璃导管代替 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com