
科目: 来源: 题型:填空题
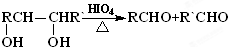
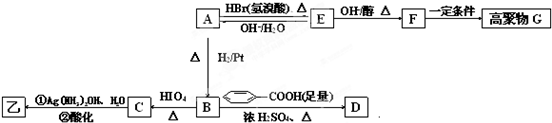
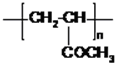 ;
;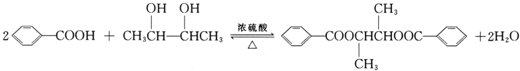 ;
;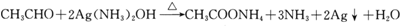 .
.查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| 实验目的 | 实验操作 | |
| A | 验证乙炔能被酸性高锰酸 钾溶液氧化 | 将电石与饱和食盐水反应生成的气体通入酸性 高锰酸钾溶液,观察溶液是否褪色 |
| B | 验证苯和液溴在FeBr3的 催化下发生取代反应 | 将反应产生的混合气体通入AgNO3溶液上方, 观察是否有淡黄色沉淀生成 |
| C | 除去乙酸乙酯中混有的少 量乙酸 | 加入足量饱和Na2CO3溶液,振荡,静置,分液, 取出上层液体 |
| D | 检验溴乙烷中的溴元素 | 取少量溴乙烷,与氢氧化钠溶液共热后加入硝 酸银溶液,观察是否出现淡黄色沉淀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. |  | |
| B. | CH3CH2CH2CHOHCH3$→_{△}^{浓硫酸}$CH3CH2CH=CHCH3+H2O | |
| C. | 2CH3CH2OH$→_{140℃}^{浓H_{2}SO_{4}}$CH3CH2OCH2CH3+H2O | |
| D. | CH3COOH+CH3OH $→_{△}^{浓H_{2}SO_{4}}$ CH3COOCH3+H2O |
查看答案和解析>>
科目: 来源: 题型:选择题
| 混合物 | 试剂 | 分离方法 | |
| A | 苯(苯酚) | 溴水 | 过滤 |
| B | 酒精(水) | 生石灰 | 蒸馏 |
| C | 苯(甲苯) | 酸性KMnO4溶液 | 分液 |
| D | 乙烷(乙烯) | Br2的CCl4溶液 | 洗气 |
| A. | A | B. | B | C. | C D.D |
查看答案和解析>>
科目: 来源: 题型:选择题
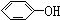 与
与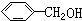
 与
与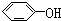
| A. | ④⑤ | B. | ①⑥ | C. | ②③ | D. | ①⑤ |
查看答案和解析>>
科目: 来源: 题型:选择题
 先进的高能量密度二次电池对下一代电动汽车的发展和可再生能源发电的有效利用具有至关重要的作用.室温Al-Mn2O4二次电池是一种新型电池,由Al3+、Al2Cl7和${AlCl}_{4}^{-}$组成的离子液体为该电池的电解液,电池结构如图所示,放电时的总反应式为Al+Mn2O4═AlMn2O4.下列说法正确的是( )
先进的高能量密度二次电池对下一代电动汽车的发展和可再生能源发电的有效利用具有至关重要的作用.室温Al-Mn2O4二次电池是一种新型电池,由Al3+、Al2Cl7和${AlCl}_{4}^{-}$组成的离子液体为该电池的电解液,电池结构如图所示,放电时的总反应式为Al+Mn2O4═AlMn2O4.下列说法正确的是( )| A. | 放电时,负极的电池反应式为AlMn2O4-3e-═Mn2O4+Al3+ | |
| B. | 放电时,Al3+向负极移动 | |
| C. | 充电时,Mn2O4极与电源的负极相连 | |
| D. | 充电时,Al电极质量增加 |
查看答案和解析>>
科目: 来源: 题型:填空题

查看答案和解析>>
科目: 来源: 题型:填空题
 已知X气体是一种无色有刺激性气味的酸性氧化物,有关X、Y、Z、W的转化关系如图所示,反应①~④均为化合反应.回答下列问题:
已知X气体是一种无色有刺激性气味的酸性氧化物,有关X、Y、Z、W的转化关系如图所示,反应①~④均为化合反应.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com