
科目: 来源: 题型:选择题
| A. | 二氧化碳和环氧丙烷在催化剂作用下可生成一种可降解的高聚物 | |
| B. | 化石燃料的燃烧和含硫金属矿石的冶炼等都是造成SO2污染的重要原因 | |
| C. | H2O2在过氧化氢酶的催化下,随着温度的升高,分解速率持续加快 | |
| D. | 氟氯烃的大量使用会破坏臭氧层,火箭、导弹将大量废气排放到高空,也会加速臭氧分解 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 参加反应的氯气的物质的量等于$\frac{1}{2}$amol | |
| B. | 改变温度,产物中KC1O3的最大理论产量为1/7amol | |
| C. | 若某温度下,反应后$\frac{c(C{l}^{-})}{c(Cl{O}^{-})}$=11,则溶液中$\frac{c(C{l}^{-})}{c(Cl{O}^{-})}$=$\frac{1}{2}$ | |
| D. | 改变温度,反应中转移电子的物质的量ne的范围:$\frac{1}{2}$amol≤ne≤$\frac{5}{6}$amol |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 多氯代甲烷中分子结构为正四面体的是二氯甲烷和四氯化碳 | |
| B. | 多氯代烷常为有机溶剂,工业上分离这些多氯代物的方法是萃取 | |
| C. | 三氟氯溴乙烯(CF3CHClBr)是一种麻醉剂,有4种同分异构体(不考虑立体异构) | |
| D. | 聚氯乙烯是生活中常用的塑料,工业上以乙烯为原料经过加成、消去和聚合反应可生成聚氯乙烯 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 通过浓硫酸除去HCl中的H2O | |
| B. | 通过灼热的镁粉除去N2中的O2 | |
| C. | 制二氧化氮时,用水或NaOH溶液吸收尾气 | |
| D. | 制氯气时,用饱和NaHCO3溶液和浓硫酸净化气体 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 玻璃容器可长期盛放各种酸 | B. | P2O5可用于干燥Cl2和NH3 | ||
| C. | Si和SiO2都用于制造光导纤维 | D. | Na2S可除去污水中的Cu2+ |
查看答案和解析>>
科目: 来源: 题型:解答题
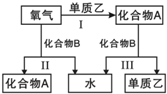 A、B是中学化学常见的化合物,它们各由两种元素组成;乙为元素R组成的单质,它们之间存在如图所示关系.根据要求回答问题:
A、B是中学化学常见的化合物,它们各由两种元素组成;乙为元素R组成的单质,它们之间存在如图所示关系.根据要求回答问题: ;其水溶液呈碱性的原因是NH3+H20
;其水溶液呈碱性的原因是NH3+H20 NH4++OH-(用离子方程式表示).
NH4++OH-(用离子方程式表示).查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 平行光照射胶体产生丁达尔现象 | B. | 紫外线照射下,液态蛋白质凝固 | ||
| C. | 电解质溶液导电过程 | D. | 铁遇到冷的浓硝酸溶液发生钝化 |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | SO32-中硫原子的杂化方式为sp3 | B. | H2O分子中氧原子的杂化方式为sp2 | ||
| C. | BF3分子呈三角锥体空间型 | D. | C2H2分子中含有3个σ键和2个π键 |
查看答案和解析>>
科目: 来源: 题型:多选题
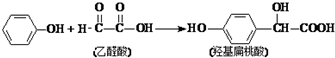
| A. | 该反应是取代反应 | |
| B. | 苯酚和羟基扁桃酸遇上FeCl3溶液都会显色 | |
| C. | 乙醛酸与H2加成的产物能在催化剂作用下形成高分子化合物 | |
| D. | 1mol羟基扁桃酸能与3mol NaOH反应 |
查看答案和解析>>
科目: 来源: 题型:解答题
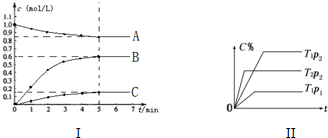
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com