
科目: 来源: 题型:多选题
| A. | 环己二烯在脱氢催化剂作用下转变为苯和氢气 | |
| B. | 溴乙烷在NaOH的乙醇溶液中的反应 | |
| C. | 乙酸和乙醇在浓硫酸的作用下生成乙酸乙酯和水 | |
| D. | 乙醛能将新制的Cu(OH)2还原成Cu2O |
查看答案和解析>>
科目: 来源: 题型:选择题
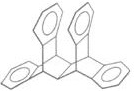 如图是一种形状酷似罗马两面神Janus的有机物结构简式如下,化学家建议将该分子叫做“Janusene”,有关Janusene的说法正确的是( )
如图是一种形状酷似罗马两面神Janus的有机物结构简式如下,化学家建议将该分子叫做“Janusene”,有关Janusene的说法正确的是( )| A. | Janusene的分子式为C30H24 | |
| B. | Janusene属于苯的同系物 | |
| C. | Janusene苯环上的一氯代物有6种 | |
| D. | Janusene既可使酸性高锰酸钾褪色,又可与H2发生加成反应 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 苯与硝酸在加热时发生取代反应,甲苯与硝酸在常温下就能发生取代反应 | |
| B. | 乙醇、苯酚都有羟基,但是电离常数不同 | |
| C. | 苯酚无需催化剂即能与溴水发生取代反应 | |
| D. | 1 mol甲苯能与3 mol H2发生加成反应 |
查看答案和解析>>
科目: 来源: 题型:解答题
 ;
;查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
| 测试时间段 | 0 | 1 | 2 | 3 | 4 |
| 雨水的pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
| 序号 | 二氧化硫的性质 | 主要操作和现象 | 化学方程式 |
| ① | 将二氧化硫通入装有品红溶液的 试管中,品红由红色变为无色 | ||
| ② | 将二氧化硫与硫化氢气体混合,出现 黄色固体. | SO2+2H2S=3S+2H2O | |
| ③ | 将二氧化硫通入装有新制氯水的试管中,氯水由浅黄绿色变为无色 |
查看答案和解析>>
科目: 来源: 题型:解答题
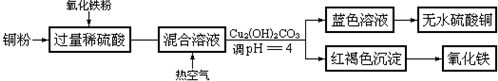
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 反应中共消耗1.8 mol H2SO4 | B. | 气体甲中SO2与H2的体积比为4:1 | ||
| C. | 反应中共消耗97.5 g Zn | D. | 反应中共转移3 mol电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com