
科目: 来源: 题型:解答题
| 序号 | 实验内容 | 实验现象 | 用离子方程式解释现象 |
| 实验Ⅰ | 向YZ的水溶液中,加入少许CCl4,逐滴滴加X单质的水溶液,振荡. | CCl4层颜色变成橙红色 | 发生反应的离子方程式是Cl2+2Br-=2Cl-+Br2. |
| 实验Ⅱ | 向上述溶液中加入少量YR的水溶液,振荡. | CCl4层颜色变成紫红色 | 发生反应的离子方程式是Br2+2I-=2Br-+I 2. |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 与W相邻的同主族元素可制成重要的半导体材料 | |
| B. | 元素的原子半径从大到小的顺序是X、Y、Z | |
| C. | WZ4分子中W、Z 原子最外层均达到8电子结构 | |
| D. | W、Y、Z元素最高价氧化物对应的水化物中酸性最强的是H2YO4 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | NaHCO3与石灰水反应当n(NaHCO3):n[Ca(OH)2]=1:1时HCO3-完全转化为CaCO3 | |
| B. | CO2通入石灰水中,当n(CO2):n[Ca(OH)2]=1:1时,能得到澄清溶液 | |
| C. | AlCl3溶液与烧碱溶液反应,当n(OH-):n(Al3+)=1:1时铝元素以AlO2-形式存在 | |
| D. | Cl2与FeBr2溶液反应,当n(Cl2):n(FeBr2)=1:1时,溶液中存在Fe2+ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 依据原子序数,推断该元素原子的核外电子数 | |
| B. | 依据相对分子质量,推断物质常温下的溶解度 | |
| C. | 依据气体的摩尔质量,推断相同状况下不同气体密度的大小 | |
| D. | 依据元素原子的最外层电子数,推测其可能的最高正价和最低化合价 |
查看答案和解析>>
科目: 来源: 题型:解答题
 A是一种常见的半导体材料,E是一种白色沉淀.存在下列物质转化关系,据此填写下列空白.
A是一种常见的半导体材料,E是一种白色沉淀.存在下列物质转化关系,据此填写下列空白.查看答案和解析>>
科目: 来源: 题型:解答题
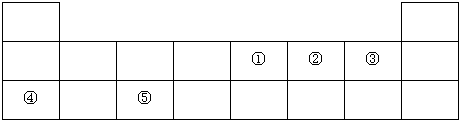
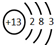 .
.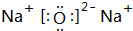 、
、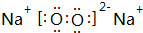 .(写两个)
.(写两个)查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Li、Be、B原子最外层电子数依次增多 | |
| B. | P、S、Cl最高正化合价依次升高 | |
| C. | F-、Cl-、Br-还原性依次减弱 | |
| D. | Na、K、Rb的金属性依次增强 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
| A. | 元素的金属性 X<Y | |
| B. | 一定条件下,Z单质与W的常见单质直接生成ZW2 | |
| C. | Y的最高价氧化物对应的水化物能溶于稀氨水 | |
| D. | 一定条件下,W单质可以将Z单质从其氢化物中置换出来 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 金属铝溶于稀硝酸中:2Al+6H+=2A13++3H2↑ | |
| B. | 碳酸钡与稀硫酸反应:Ba2++SO42-=BaSO4↓ | |
| C. | 碳酸氢钠溶液与少量盐酸反应:CO32-+2 H+=H2O+CO2↑ | |
| D. | 碳酸钠溶液缓慢滴入少量稀盐酸:CO32-+H+=HCO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com