
科目: 来源: 题型:选择题
| A. | 若容器中X2全部转化为它的同素异形体X3,那么X3的分子量有3种 | |
| B. | 质量数为16的一种核素在此容器中的原子百分数为80% | |
| C. | 只要容器中同位素组成不变,X原子在任何条件下发生重新组合,最后得到三种X2,分子数之比总是15:4:1 | |
| D. | 此容器中X2的平均分子量是32.6 |
查看答案和解析>>
科目: 来源: 题型:填空题
 如图所示,组成一种原电池.试回答下列问题(灯泡功率合适):
如图所示,组成一种原电池.试回答下列问题(灯泡功率合适):查看答案和解析>>
科目: 来源: 题型:解答题
 .
. .
.查看答案和解析>>
科目: 来源: 题型:解答题

 CH3COOCH2CH2CH3+H2O.
CH3COOCH2CH2CH3+H2O. 或
或 .
. .
.查看答案和解析>>
科目: 来源: 题型:填空题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
 .元素⑩名称为溴在周期表中的位置第四周期第ⅦA族.
.元素⑩名称为溴在周期表中的位置第四周期第ⅦA族. .
. ,该化合物属于离子(填“共价”或“离子”)化合物.
,该化合物属于离子(填“共价”或“离子”)化合物. ,该化合物是由极性共价键(填“极性”、“非极性”)键形成的.
,该化合物是由极性共价键(填“极性”、“非极性”)键形成的.
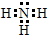 ;该氢化物常温下和元素②的最高价氧化物对应水化物反应的化学方程式为NH3+HNO3═NH4NO3.
;该氢化物常温下和元素②的最高价氧化物对应水化物反应的化学方程式为NH3+HNO3═NH4NO3.查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
| 族 周期 | ⅠA | 0 | ||||||
| ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 2He | ||
| 1 | A | |||||||
| 2 | B | C | D | |||||
| 3 | E | F | G | H | I | J | K | L |
查看答案和解析>>
科目: 来源: 题型:填空题
| I A | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | |
| 2 | C | D | |||||
| 3 | A | B | E | F |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com