
科目: 来源: 题型:选择题
| A. | 单位时间内生成n mol A,同时生成2n mol C | |
| B. | A、B、C的浓度相等 | |
| C. | 单位时间内生成n mol A,同时生成3n mol B | |
| D. | A、B、C的分子数之比为1:3:2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 2HgO $\frac{\underline{\;\;△\;\;}}{\;}$2Hg+O2↑ | B. | 2A12O3 $\frac{\underline{\;电解\;}}{\;}$4Al+3O2↑ | ||
| C. | H2+Na2O $\frac{\underline{\;高温\;}}{\;}$2Na+H2O | D. | 4 CO+Fe3O4$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2 |
查看答案和解析>>
科目: 来源: 题型:填空题
 +3HNO3 $→_{△}^{浓硫酸}$
+3HNO3 $→_{△}^{浓硫酸}$ +3H2O.
+3H2O.查看答案和解析>>
科目: 来源: 题型:填空题
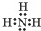 ;NH3在同族元素形成的氢化物中具有较高的沸点,其原因是NH3分子间有氢键.
;NH3在同族元素形成的氢化物中具有较高的沸点,其原因是NH3分子间有氢键.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | SO2既可做氧化剂,又可做还原剂 | |
| B. | SO2是硫酸的酸酐 | |
| C. | 大气中SO2的主要来源是汽车排出的尾气 | |
| D. | SO2具有漂白性,因而可以使石蕊试液褪色 |
查看答案和解析>>
科目: 来源: 题型:解答题
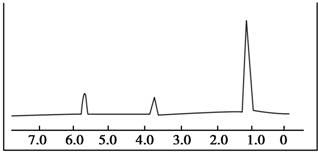
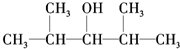 B.
B.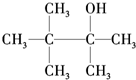 C.
C.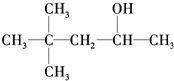
查看答案和解析>>
科目: 来源: 题型:填空题
 .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 若完全燃烧,1 mol雄酮(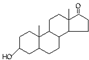 )比雌酮( )比雌酮(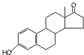 )多消耗2 mol O2 )多消耗2 mol O2 | |
| B. | 苯分子中的一个碳原子被一个氮原子代替,则新分子的式量为79 | |
| C. | 蔗糖、麦芽糖和乳糖的分子式都为C12H22O11,均能发生银镜反应 | |
| D. | 只用溴水一种试剂不能鉴别甲苯、己烯、乙醇、四氯化碳四种液体 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 乙醇和乙酸都存在羟基 | |
| B. | 甲烷和甲苯都可以与氯气反应 | |
| C. | 高锰酸钾可以氧化甲苯和乙醛 | |
| D. | 乙烯可以发生加成反应,苯不能发生加成反应 |
查看答案和解析>>
科目: 来源: 题型:填空题
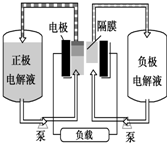 全钒液流电池是一种活性物质呈循环流动液态的电池,目前钒电池技术已经趋近成熟.
全钒液流电池是一种活性物质呈循环流动液态的电池,目前钒电池技术已经趋近成熟.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com