
科目: 来源: 题型:选择题
| A. | pH=1的溶液中:Na+、NH4+、SO42-、ClO- | |
| B. | KW/c(H+)=0.1 mol•L-1的溶液中:Na+、K+、MnO4-、HCO3- | |
| C. | 0.1 mol•L-1的Na2SO3溶液中:K+、H+、SO42-、NO3- | |
| D. | 澄清透明的溶液中:Fe3+、Na+、Cl-、SO42- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | NaOH的电子式: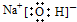 | |
| B. | 质子数和中子数均为16的硫原子:1616S | |
| C. | 氟原子的结构示意图: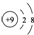 | |
| D. | 乙醛的结构简式: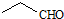 |
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | H2S是一种弱电解质 | |
| B. | 可用石灰乳吸收H2S气体 | |
| C. | 根据如图可知FeCl3、CuCl2均能氧化H2S | |
| D. | H2S在空气中燃烧可以生成SO2 |
查看答案和解析>>
科目: 来源: 题型:解答题
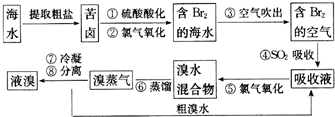
查看答案和解析>>
科目: 来源: 题型:解答题
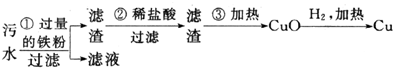
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 向盛有少量Mg(OH)2沉淀的试管中滴加适量NH4Cl溶液,沉淀溶解:Mg(OH)2+2NH4+═2NH3•H2O+Mg2+ | |
| B. | SO2通入澄清石灰水中,产生白色沉淀:SO2+Ca2++2OH-═CaSO4↓+H2O | |
| C. | 向Ca(HCO3)2溶液中加入过量NaOH溶液,有白色沉淀生成:Ca2++2 HCO3-+2 OH-═CaCO3↓+CO32-+2H2O | |
| D. | 长期过量服用阿司匹林出现水杨酸(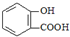 )反应,可静脉注滴NaHCO3溶液: )反应,可静脉注滴NaHCO3溶液: |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 向氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| B. | 向次氯酸钙溶液中通入过量CO2:2ClO-+Ca2++H2O+CO2═2HClO+CaCO3↓ | |
| C. | 向含0.015 molNaOH的溶液中通入0.64 g SO2:3OH-+2SO2═SO32-+HSO3-+H2O | |
| D. | 向Fe(OH)2中加入足量稀硝酸:Fe(OH)2+2H+═Fe2++2H2O |
查看答案和解析>>
科目: 来源: 题型:解答题
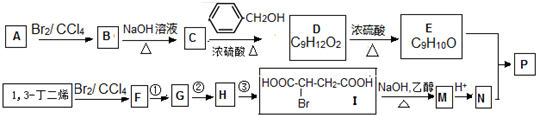
 ,
,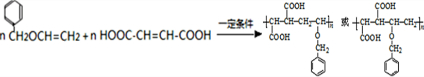 高聚物P的亲水性比由E形成的聚合物强(填“强、弱”).
高聚物P的亲水性比由E形成的聚合物强(填“强、弱”).
查看答案和解析>>
科目: 来源: 题型:解答题

 ;其所含化学键类型为共价键、离子键;
;其所含化学键类型为共价键、离子键;查看答案和解析>>
科目: 来源: 题型:选择题
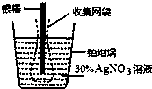 下图为根据电解原理制成“银电量计”.其原理是:通过测定电解过程中附着在惰性电极上金属质量,计算通过电解池的电量.下列说法正确的是( )
下图为根据电解原理制成“银电量计”.其原理是:通过测定电解过程中附着在惰性电极上金属质量,计算通过电解池的电量.下列说法正确的是( )| A. | 电量计工作时溶液里的阴离子向正极移动 | |
| B. | 电量计工作时银棒应与电源的正极相连 | |
| C. | 网袋是收集银溶解过程中产生的金属颗粒,若没有该网袋,测量结果会偏低 | |
| D. | 若得金属银的沉积量为1.08g,则电解过程中转移的电子为0.01mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com