
科目: 来源: 题型:解答题
 现用如图装置来测定某原电池工作时在某段时间内通过导线的电子的物质的量.量筒的规格为1000mL,供选择的电极材料有纯铜片和纯锌片.请回答下列问题:
现用如图装置来测定某原电池工作时在某段时间内通过导线的电子的物质的量.量筒的规格为1000mL,供选择的电极材料有纯铜片和纯锌片.请回答下列问题:查看答案和解析>>
科目: 来源: 题型:解答题
| A | |||||||
| B | C | D | |||||
| E | F | G | |||||
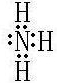 .
.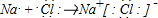 .
.查看答案和解析>>
科目: 来源: 题型:解答题
 K2S
K2S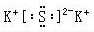 NaOH
NaOH
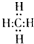 ,分子里各原子的空间分布呈正四面体结构.分子式为C4Hm的烷烃,m值等于10;并写出它的同分异构体的结构简式CH3CH2CH2CH3、(CH3)2CHCH3.
,分子里各原子的空间分布呈正四面体结构.分子式为C4Hm的烷烃,m值等于10;并写出它的同分异构体的结构简式CH3CH2CH2CH3、(CH3)2CHCH3.查看答案和解析>>
科目: 来源: 题型:选择题
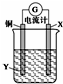
| A. | X可以是银或石墨 | B. | 电子从铜电极经外电路流向X电极 | ||
| C. | Y是硫酸铜溶液 | D. | X极上的电极反应式为Ag++e-═Ag |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①③ | B. | ①②④ | C. | ①②③④ | D. | ①③④ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 乙醇催化氧化制乙醛 | B. | 乙醇与浓硫酸共热制乙烯 | ||
| C. | 苯乙烯在一定条件下制聚苯乙烯 | D. | 溴乙烷制乙醇 |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:填空题
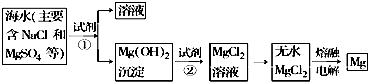
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com