
科目: 来源: 题型:选择题
| A. | 工业电解饱和食盐水:2Cl-+H2O=Cl2↑+H2↑+OH- | |
| B. | 碳酸钠的水解:CO32-+2H2O═H2CO3+2OH- | |
| C. | 硫酸铝溶液中滴加过量浓氨水:Al3++4 NH3•H2O═AlO${\;}_{2}^{-}$+4NH4++2H2O | |
| D. | 用过氧化氢从酸化海带灰浸出液中提取碘:2I-+H2O2+2H+=I2+2H2O |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Ba2+、AlO2-、NO3-、Cl- | B. | K+、Na+、ClO-、Fe2+ | ||
| C. | Na+、I-、NO3-、SO42- | D. | NH4+、Na+、S2-、CO32- |
查看答案和解析>>
科目: 来源: 题型:解答题
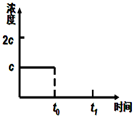 请你利用所学反应原理知识解决下列问题:
请你利用所学反应原理知识解决下列问题:查看答案和解析>>
科目: 来源: 题型:解答题
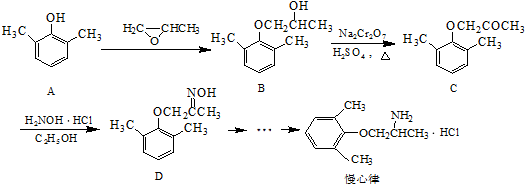
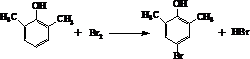 .
. .
.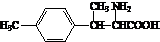 .
.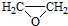 ).写出以邻甲基苯
).写出以邻甲基苯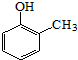 )和乙醇为原料制备
)和乙醇为原料制备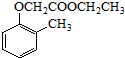 的合成路线流程图(无机试
的合成路线流程图(无机试查看答案和解析>>
科目: 来源: 题型:多选题

| A. | X、Y、Z三种元素最低价氢化物的沸点依次升高 | |
| B. | 由X、Y和氢三种元素形成的化合物中只有共价键 | |
| C. | 原子半径:W>X>Y | |
| D. | T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 编号 | 叙述I | 叙述II |
| A | Fe3+的氧化性比Cu2+强 | FeCl3溶液可用于溶解回收旧电路板中的铜 |
| B | NH4Cl受热分解 | 加热可将Ca(OH)2和NH4Cl固体混合物分离 |
| C | 金属活动性铜比铁弱 | 镀铜铁制品表层划损后仍然受到保护 |
| D | Cl2具有漂白性 | 用氯气制盐酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1mol苯中含有3nA个碳碳双键 | |
| B. | 室温下,1LpH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA | |
| C. | 氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA | |
| D. | 一定条件下2 mol SO2和1 mol O2充分反应后,混合气体的分子总数大于2NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | K+、Al3+、CO32-、Cl- | B. | Na+、H+、SO42-、SiO32- | ||
| C. | H+、NH4+、SO42-、I- | D. | H+、Fe2+、Cl-、ClO- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 青铜器、硬币都属于纯净物 | |
| B. | 葡萄糖和银氨溶液发生银镜反应可用作制镜子 | |
| C. | 铺路用的沥青主要含有C、H、O等元素 | |
| D. | 鸡蛋清中加入胆矾可以使蛋白质发生盐析 |
查看答案和解析>>
科目: 来源: 题型:解答题
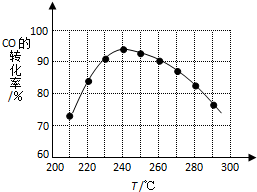 二甲醚(CH3OCH3)在未来可能替代柴油和液化气作为洁净液体燃料使用.工业上以CO和H2为原料生产CH3OCH3的新工艺主要发生三个反应:
二甲醚(CH3OCH3)在未来可能替代柴油和液化气作为洁净液体燃料使用.工业上以CO和H2为原料生产CH3OCH3的新工艺主要发生三个反应:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com