
科目: 来源: 题型:解答题
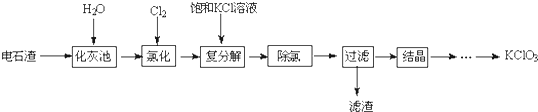
| 几种物质溶解度与温度的关系 | |||||
| 温度 | 0 | 10 | 20 | 30 | 40 |
| S(CaCl2)/g | 59.5 | 64.7 | 74.5 | 100 | 128 |
| S[Ca(ClO3)2]/g | 209 | ||||
| S(KClO3)/g | 3.3 | 5.2 | 7.3 | 10.2 | 13.9 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 滴定 次数 | 待测溶液的 体积/mL | 标准溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
查看答案和解析>>
科目: 来源: 题型:填空题
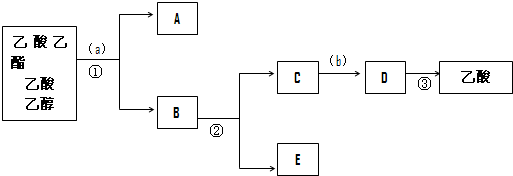
| 物质 | 熔点/℃ | 沸点/℃ | 密度/(g/cm3) |
| 乙醇 | -144 | 78 | 0.789 |
| 乙酸 | 16.6 | 117.9 | 1.05 |
| 乙酸乙酯 | -83.6 | 77.5 | 0.90 |
| 浓硫酸 | -- | 338 | 1.84 |
查看答案和解析>>
科目: 来源: 题型:解答题
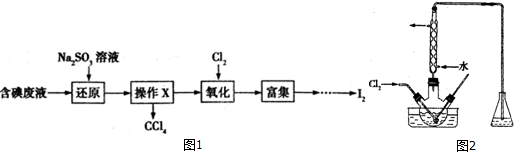
查看答案和解析>>
科目: 来源: 题型:解答题
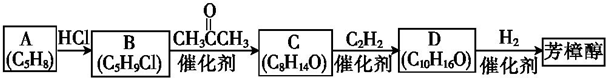
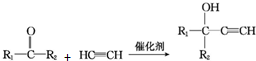 (R1、R2均为烃基)
(R1、R2均为烃基)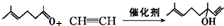 ,该反应类型为加成反应.
,该反应类型为加成反应.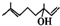 .
.查看答案和解析>>
科目: 来源: 题型:填空题
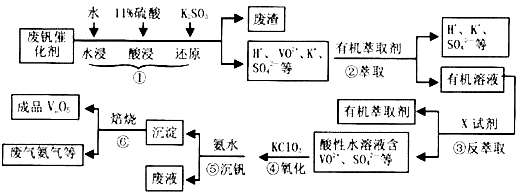
| pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| 钒沉淀率/% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | 有机物A不能使溴的四氯化碳溶液褪色 | |
| B. | 胡妥油可以发生加成反应和氧化反应 | |
| C. | 有机物A与胡妥油互为同系物 | |
| D. | 1 mol胡妥油完全燃烧消耗313.6 L的氧气 |
查看答案和解析>>
科目: 来源: 题型:选择题
| X | Y | ||
| Z | W |
| A. | X元素Z能形成气态氢化物XH3 | B. | Z与W形成的化合物在熔融时能导电 | ||
| C. | 自然界存在大量的单质Z | D. | X与Y形成的化合物不超过3种 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Al是不活泼的金属,故铝可制成铝箔包装物品 | |
| B. | NaHCO3能与碱反应,故NaHCO3可以用于制作糕点 | |
| C. | NH3能与Cl2生成NH4Cl,故可用浓氨水检验输送氯气的管道是否有泄漏 | |
| D. | 明矾与K2FeO4都能与水生成胶体,均可用于水的净化、杀菌和消毒 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com