
科目: 来源: 题型:选择题
| 化学键 | H2(g) | Br2(g) | HBr(g) |
| 断裂1mol化学键需要吸收的能量/kJ | 436 | a | 369 |
| A. | 404 | B. | 260 | C. | 230 | D. | 200 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 它们的原子核外电子层数随核电荷数的增多而增多 | |
| B. | 单质的颜色随核电荷数的增多而加深 | |
| C. | 被其它卤素单质从其卤化物中置换出来的可能性随核电荷数的增多而增大 | |
| D. | 它们的氢化物的稳定性随核电荷数的增多而增强 |
查看答案和解析>>
科目: 来源: 题型:填空题
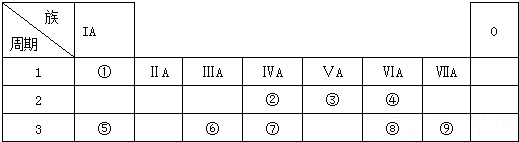
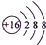
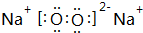 ,含有的化学键类型有离子键、共价键
,含有的化学键类型有离子键、共价键查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 6:1 | B. | 12:1 | C. | 1:1 | D. | 1:2 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
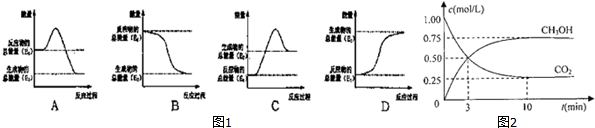
查看答案和解析>>
科目: 来源: 题型:解答题
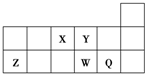
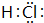 ,把它溶于水,由于共价键受到破坏而电离出H+和Q-,使溶液呈酸性.结构类型相同Y、W的氢化物的沸点从高到低排列次序是(填化学式)H2O>H2S.
,把它溶于水,由于共价键受到破坏而电离出H+和Q-,使溶液呈酸性.结构类型相同Y、W的氢化物的沸点从高到低排列次序是(填化学式)H2O>H2S.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | K+、NH4+、OH-、SO42- | B. | H+、Fe2+、SO42-、ClO- | ||
| C. | Na+、Ca2+、Cl-、CO32- | D. | K+、Ca2+、Cl-、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com