
科目: 来源: 题型:选择题
| A. | c(IO3-)、c(HSO3-)逐渐增大 | B. | c(K+)逐渐增大,反应速率加快 | ||
| C. | 溶液的pH减小,IO3-的氧化性增强 | D. | c(H+)增大,反应速率加快 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 14g | B. | 47g | C. | 54g | D. | 94g |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 2-甲基丁烷与正丁烷的一氯取代产物的种类相同 | |
| B. | 分子式为C4H8O2且含 基团的同分异构体共有4种 基团的同分异构体共有4种 | |
| C. | 与CH2═CHCH3与HCl发生加成反应可得到2种有机物 | |
| D. | 分子式C8H10的苯的同系物共有3种结构 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | T、W、M的最高价氧化物的水化物相互反应 | |
| B. | T、Y、W组成的化合物溶于含酚酞的水,溶液显红色 | |
| C. | 简单离子半径:r(W)>r(M)>r(Y)>r(X) | |
| D. | 简单氢化物的稳定性:X>T>Y |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:填空题
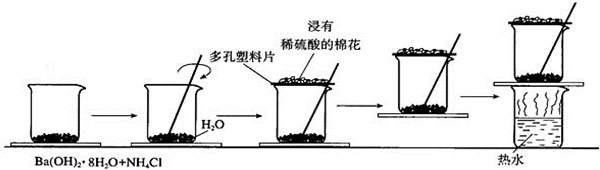
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com