
科目: 来源: 题型:解答题
| 时间 物质 | 0 min | 10 min | 30 min | 60 min | 70 min |
| CO2(mol/L) | 0 | 0.2 | 0.6 | 0.8 | 0.8 |
| CH3OH(mol/L) | 1.0 | 0.8 | 0.4 | 0.2 | 0.2 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 酸性高锰酸钾溶液中滴入少量过氧化氢:2MnO4-+3H2O2+6H+═2Mn2++4O2↑+6H2O | |
| B. | 0.03mol/L NH4Al(SO4)2溶液与0.05mol/l Ba(OH)2溶液等体积混合:NH4++3Al3++5SO42-+5Ba2++10 OH-═5BaSO4↓+3Al(OH)3↓+NH3•H2O | |
| C. | 向烧碱溶液中加少量Ca(HCO3)2溶液:HCO3-+Ca2+OH-=CaCO3↓+2H2O | |
| D. | 在强碱溶液中次氯酸钠与氢氧化铁反应生成:3ClO-+2Fe(OH)3=2FeO42-+3Cl-+H2O+4H+ |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1.5mol | B. | 2mol | C. | 2.5mol | D. | 4mol |
查看答案和解析>>
科目: 来源: 题型:解答题
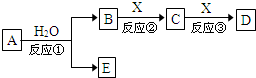 由短周期元素组成的中学常见物质A、B、C、D、E存在图转化关系(部分生成物和反应条件略).
由短周期元素组成的中学常见物质A、B、C、D、E存在图转化关系(部分生成物和反应条件略).查看答案和解析>>
科目: 来源: 题型:选择题
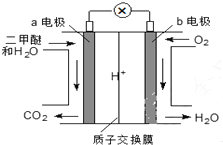 二甲醚(CH3OCH3)是一种绿色、可再生的新能源.右图是绿色电源“燃料电池”的工作原理示意图(a、b均为多孔Pt电极).该电池工作时,下列说法不正确的是( )
二甲醚(CH3OCH3)是一种绿色、可再生的新能源.右图是绿色电源“燃料电池”的工作原理示意图(a、b均为多孔Pt电极).该电池工作时,下列说法不正确的是( )| A. | a电极为该电池负极 | |
| B. | O2在b电极上反应为O2+2H2O+4e-=4OH- | |
| C. | 电池工作时,若a电极上有1molCH3OCH3放电,电路中有12mol电子转移 | |
| D. | 电池工作时,电池内部H+从a电极移向b电极 |
查看答案和解析>>
科目: 来源: 题型:解答题
 氟是电负性最大的非金属元素,又因其半径较小,极易和金属元素反应,并将它们氧化到最高价态,生成MnF7、VF5、CaF2等.氟还可以和氧形成一系列的氟化物,如OF2、O2F2、O4F2等.请回答下列问题:
氟是电负性最大的非金属元素,又因其半径较小,极易和金属元素反应,并将它们氧化到最高价态,生成MnF7、VF5、CaF2等.氟还可以和氧形成一系列的氟化物,如OF2、O2F2、O4F2等.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com