
科目: 来源:2017届江西省鹰潭市高三上学期第四次月考化学试卷 题型:选择题
下列说法在一定条件下可以实现的是
①酸性氧化物与碱发生反应
②弱酸与盐溶液反应可以生成强酸
③没有水生成,也没有沉淀和气体生成的复分解反应
④两种酸溶液充分反应后的溶液体系为中性
⑤有单质参加的非氧化还原反应⑥两种氧化物反应的产物有气体
A.①②③④⑤⑥
B.①②⑤⑥
C.①②③⑤
D.①②③⑤⑥
查看答案和解析>>
科目: 来源:2017届江西省鹰潭市高三上学期第四次月考化学试卷 题型:选择题
下列有关实验原理、装置、操作或结论的描述中,正确的(或实验能达到预期目的)有(有关装置中的夹持仪器略去未画)( )项
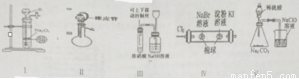
Ⅰ.仿启普发生器制少量氧气Ⅱ.该装置检查气密性(止水夹已关)一打开分液漏斗活塞,液体顺利流下Ⅲ.进行铜与浓硝酸反应的实验Ⅳ.证明氧化性Cl2>Br2>I2Ⅴ.验证酸性的强弱,H2SO4>H2CO3>HClO
A.1项
B.2项
C.3项
D.4项
查看答案和解析>>
科目: 来源:2017届江西省鹰潭市高三上学期第四次月考化学试卷 题型:选择题
向铁铜合金中加入硝酸溶液恰好完全反应,得到NO2、N2O4、NO混合气体,向反应后溶液中加入2mol/LNaOH溶液,至沉淀恰好完全。若将得到的NO2、N2O4、NO混合气体,与2.24L(标准状况下)O2混合后通入水中恰好被完全吸收生成硝酸。则反应中消耗的NaOH溶液的体积是
A.150ml
B.180ml
C.200ml
D.250ml.
查看答案和解析>>
科目: 来源:2017届江西省鹰潭市高三上学期第四次月考化学试卷 题型:实验题
锌是一种过渡金属,外观呈现银白色,在现代工业中对于电池制造上有不可磨灭的地位。现代炼锌的方法可分为火法和湿法两大类.硫酸铅是生产锌的副产品。
(1)火法炼锌是将闪锌矿(主要含ZnS)通过浮选、焙烧使它转化为氧化锌,再把氧化锌和焦炭混合,在鼓风炉中加热至1473-1573K,使锌蒸馏出来。将闪锌矿焙烧使它转化为氧化锌的主要化学反应方程式为。
(2)某含锌矿的主要成分为ZnS(还含少量FeS等其他成分),以其为原料冶炼锌的工艺流程如图所示:

回答下列问题:
①焙烧过程中产生的含尘烟气可净化制酸,该酸可用于后续的_______操作。
②浸出液“净化”过程中加入的主要物质为锌粉,其作用是。
③改进的锌冶炼工艺,采用了“氧压酸浸”的全湿法流程,既省略了易导致空气污染的焙烧过程,又可获得一种有工业价值的非金属单质。“氧压酸浸”中发生的主要反应的离子方程式为________
(3)工业冶炼锌的过程中,会产生铅浮渣(主要成分是PbO、Pb,还含有少量Ag、Zn、CaO和其他不溶于硝酸的杂质),某科研小组研究利用铅浮渣生产硫酸铅的流程如下:

已知:25℃时,Ksp(CaSO4)=4.9×10-5,KSP(PbSO4)=1.6×10-8。
①已知步骤Ⅰ有NO气体产生,浸出液中含量最多的阳离子是Pb2+。写出Pb参加反应的化学方程式_____________________。
②步骤Ⅰ需控制Pb的用量并使Pb稍有剩余,目的是使Ag留在浸出渣中,产品PbSO4还需用Pb(NO3)2溶液多次洗涤,目的是除去附着在硫酸铅表面的微溶物硫酸钙。沉淀转化反应的离子方程式是___。
③母液中可循环利用的溶质的化学式是_____________(填一种物质)
(4)现向含Pb2+、Ca2+浓度均为0.10mol/L的混合溶液中滴加0.10mol/LSO42-溶液.当Pb2+沉淀完全时,溶液中Ca2+浓度为mol/L
查看答案和解析>>
科目: 来源:2017届江西省鹰潭市高三上学期第四次月考化学试卷 题型:简答题
(14分)发展洁净煤技术、利用CO2制备清洁能源等都是实现减碳排放的重要途径。
(1)将煤转化成水煤气的反应:C(s)+H2O(g) CO(g)+H2(g)可有效提高能源利用率,若在上述反应体系中加入催化剂(其他条件保持不变),此反应的△H________(填“增大”、“减小”或“不变”),判断的理由是________。
CO(g)+H2(g)可有效提高能源利用率,若在上述反应体系中加入催化剂(其他条件保持不变),此反应的△H________(填“增大”、“减小”或“不变”),判断的理由是________。
(2)CO2制备甲醇:CO2(g)+3H2(g)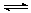 CH3OH(g)+H2O(g)ΔH=-49.0kJ·mol-1,在体积为1L的密闭容器中,充入1molCO2和3molH2,测得CO2(g)和CH3OH(g)浓度随时间变化如右图所示。
CH3OH(g)+H2O(g)ΔH=-49.0kJ·mol-1,在体积为1L的密闭容器中,充入1molCO2和3molH2,测得CO2(g)和CH3OH(g)浓度随时间变化如右图所示。
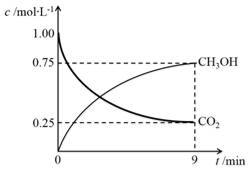
①该反应化学平衡常数K的表达式是________。
②0~9min时间内,该反应的平均反应速率ν(H2)=________。
③在相同条件下,密闭容器的体积缩小至0.5L时,此反应达平衡时放出的热量(Q)可能是________(填字母序号)kJ。
a.0<Q<29.5
B.29.5<Q<36.75
C.36.75<Q<49
D.49<Q<98
④在一定条件下,体系中CO2的平衡转化率(α)与L和X的关系如右图所示,L和X分别表示温度或压强。
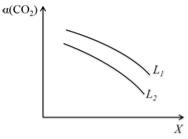
X表示的物理量是。判断L1与L2的大小关系。
(3)科学家用氮化镓材料与铜组装如右图的人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4.

写出铜电极表面的电极反应式,为提高该人工光合系统的工作效率,可向装置中加入少量(选填“盐酸”或“硫酸”).
(4)利用CO2和NH3为原料也合成尿素,在合成塔中的主要反应可表示如下:
反应①:2NH3(g)+CO2(g)=NH2CO2NH4(s)△H1=__________________
反应②:NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g)△H2=+72.49kJ·mol-1
总反应:2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g)△H=-86.98kJ·mol-1;
则反应①的△H1=_______________。
(5)现将amol铁和bmol铜的混合物与含有cmolHNO3的稀溶液充分反应,设还原产物为NO。下列结论不正确的是(填序号)
A.若剩余金属0.5amol,则氧化产物为一种或二种
B.若只有一种氧化产物,则3c=8a
C.若有二种氧化产物,被还原的硝酸物质的量为0.25cmol
D.若有三种氧化产物,被还原的硝酸物质的量为0.25cmol
查看答案和解析>>
科目: 来源:2017届江西省鹰潭市高三上学期第四次月考化学试卷 题型:实验题
氯化铁是常见的水处理剂,利用废铁屑可制备无水氯化铁。实验室制备装置和工业制备流程图如下:
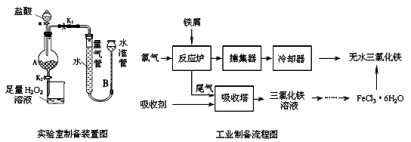
已知:(1)无水FeCl3的熔点为555K、沸点为588K。
(2)废铁屑中的杂质不与盐酸反应
(3)不同温度下六水合氯化铁在水中的溶解度如下:
温度/℃ | 0 | 20 | 80 | 100 |
溶解度(g/100gH2O) | 74.4 | 91.8 | 525.8 | 535.7 |
实验室制备操作步骤如下:
Ⅰ.打开弹簧夹K1,关闭弹簧夹K2,并打开活塞a,缓慢滴加盐酸。
Ⅱ.当时,关闭弹簧夹K1,打开弹簧夹K2,当A中溶液完全进入烧杯后关闭活塞a。
Ⅲ.将烧杯中溶液经过一系列操作后得到FeCl3·6H2O晶体。
请回答:
(1)烧杯中足量的H2O2溶液的作用是。
(2)为了测定废铁屑中铁的质量分数,操作Ⅱ中“……”的内容是__________。
(3)从FeCl3溶液制得FeCl3•6H2O晶体的操作步骤是:加入后、蒸发浓缩、冷却结晶、过滤、洗涤、干燥.
(4)试写出吸收塔中反应的离子方程式:。
(5)捕集器温度超过673K时,存在相对分子质量为325的铁的氯化物,该物质的分子式为。
(6)FeCl3的质量分数通常可用碘量法测定:称取mg无水氯化铁样品,溶于稀盐酸,配制成100mL溶液;取出10.00mL,加入稍过量的KI溶液,充分反应后,滴入几滴淀粉溶液,并用cmol•L-1Na2S2O3溶液滴定,消耗VmL(已知:I2+2S2O32-═2I-+S4O62-)。
①滴定过程中可能造成实验结果偏低的是
A.锥形瓶未润洗
B.锥形瓶中溶液变色后立刻停止滴定,进行读数
C.滴定管尖嘴内滴定前无气泡,滴定终点发现气泡
D.滴定终点时仰视读数
②样品中氯化铁的质量分数
查看答案和解析>>
科目: 来源:2017届江西省鹰潭市高三上学期第四次月考化学试卷 题型:推断题
芳香酯Ⅰ的合成路线如下:
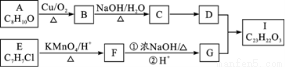
A.C8H16OE.C7H7ClI.C23H22O3
已知以下信息:①A—I均为芳香族化合物,B能发生银镜反应,D的相对分子质量比C大4,E的核磁共振氢谱有3组峰。②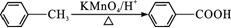
③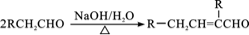
请回答下列问题:
(1)A→B的反应类型为,D所含官能团的名称为,E的名称为。
(2)E→F与F→G的顺序能否颠倒(填“能”或“否”),理由.
(3)B与银氨溶液反应的化学方程式为。
(4)I的结构简式为。
(5)符合下列要求A的同分异构体还有种。
①与Na反应并产生H2②芳香族化合物
(6)根据已有知识并结合相关信息,写出以CH3CH2OH为原料制备CH3CH2CH2CH2OH的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
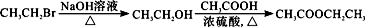
查看答案和解析>>
科目: 来源:2016-2017学年河北石家庄辛集中学高二上阶段考一化学卷(解析版) 题型:选择题
下列物质的水溶液能导电,但属于非电解质的是( )
A.CH3COOH B.Cl2 C.NH4HCO3 D.SO2
查看答案和解析>>
科目: 来源:2016-2017学年河北石家庄辛集中学高二上阶段考一化学卷(解析版) 题型:选择题
下列说法正确的是( )
A.配制FeCl3溶液时,将FeCl3固体溶于适量盐酸中,然后再用水稀释到所需的浓度
B.为绘制中和滴定曲线,在滴定过程中,每隔相同时间用pH计测定一次锥形瓶中溶液的pH
C.测定溶液的pH时,应先将pH试纸润湿,然后进行检测
D.为准确测定盐酸与NaOH溶液反应的中和热,所用酸和碱的物质的量应相等
查看答案和解析>>
科目: 来源:2016-2017学年河北石家庄辛集中学高二上阶段考一化学卷(解析版) 题型:选择题
有一支50 mL酸式滴定管中盛有盐酸,液面恰好在a mL刻度处,把管内液体全部放出,盛量筒内,所得液体体积一定是( )
A.a mL B.(50-a) mL C.大于(50-a) mL D.大于a mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com