
科目: 来源: 题型:选择题
| A. | 澄清透明的溶液中:MnO4-、SO42-、K+、Fe3+ | |
| B. | 0.1 mol•L-1FeCl3溶液中:Mg2+、NH4+、SCN-、SO42- | |
| C. | 滴入甲基橙显黄色的溶液中:Na+、ClO-、I-、SO42- | |
| D. | 水电离产生的c(H+)=10-12 mol•L-1的溶液中:K+、Na+、NO3-、CH3COO- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | HClO的结构式:H-Cl-O | |
| B. | NaHCO3在水中的电离方程式:NaHCO3=Na++H++CO32- | |
| C. | 羟基的电子式: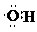 | |
| D. | 异丙醇的结构简式:CH3CH2CH2OH |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
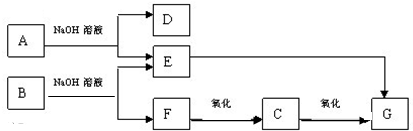
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | C7H15OH | B. | C6H13OH | C. | C5H12OH | D. | C2H5OH |
查看答案和解析>>
科目: 来源: 题型:解答题
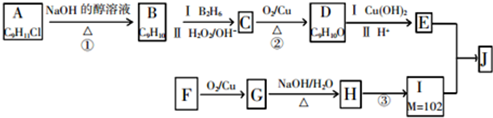
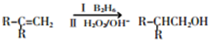
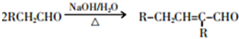
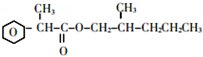 .
.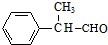 +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$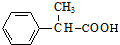 +Cu2O↓+2H2O.
+Cu2O↓+2H2O.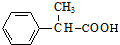 +CH3CH2CH2CH2CH(CH3)OH$→_{△}^{浓硫酸}$
+CH3CH2CH2CH2CH(CH3)OH$→_{△}^{浓硫酸}$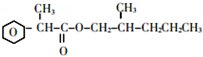 +H2O.F→G的化学方程式2CH3CH2CH2OH+O2$→_{△}^{Cu}$2CH3CH2CHO+2H2O.
+H2O.F→G的化学方程式2CH3CH2CH2OH+O2$→_{△}^{Cu}$2CH3CH2CHO+2H2O.查看答案和解析>>
科目: 来源: 题型:解答题
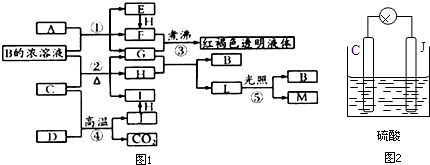
查看答案和解析>>
科目: 来源: 题型:选择题
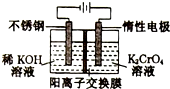 以铬酸钾(右室起始加入0.4molK2CrO4)为原料,电化学法制备重铬酸钾的实验装置示意图如图,下列说法正确的是( )
以铬酸钾(右室起始加入0.4molK2CrO4)为原料,电化学法制备重铬酸钾的实验装置示意图如图,下列说法正确的是( )| A. | 在阳极室,通电后溶液逐渐由橙色变为黄色 | |
| B. | 电路中有0.2mol电子通过时,阳极与阴极溶液减少的质量差为1.4g | |
| C. | 若测得右室中K与Cr的物质的量之比为3:2,则此过程电路中共转移电子数为0.1NA | |
| D. | 若测定阳极液中K与Cr的物质的量之比为d,则此时铬酸钾的转化率为2-d |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Na2CO3溶液加水稀释后,恢复至原温度,pH和Kw均减小 | |
| B. | NH4Cl、CH3COONa、NaHCO3、NaHSO3溶于水,对水的电离都有促进作用 | |
| C. | 浓度均为0.10mol•L-1 NH4Cl和NH4HSO4溶液,c(NH4+)前者大于后者 | |
| D. | 可用Na2CO3溶液处理水垢中的CaSO4,转化为易于除去的CaCO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com