
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
 A~J为中学化学中常见的几种物质.它们有如图转化关系:
A~J为中学化学中常见的几种物质.它们有如图转化关系:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 检气管法是按照反应①原理设计的 | |
| B. | 检气管法是按照反应②原理设计的 | |
| C. | 反应①②均可以设计成检气管法,但考虑到相同量KIO3①消耗SO2少,所以检气管法是按①设计的 | |
| D. | 反应①②均可以设计成检气管法,但考虑到相同量KIO3②消耗SO2多,所以检气管法是按②设计的 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 碳酸氢镁溶液中加入过量石灰水:Mg2++2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+MgCO3↓ | |
| B. | 1mo•L-1 的 NaAlO2 溶液和2.5mol•L-1 的盐酸等体积混合:2AlO2-+5 H+=Al(OH)3↓+Al3++H2 O | |
| C. | 亚硫酸氢钡溶液中加入适量双氧水:HSO3-+H2O2=SO42-+H2O+H+ | |
| D. | 硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液:Fe2++2H++H2O2=Fe3++2H2O |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 在标准状况下,2.24 L二氧化硫与氧气混合气体中所含氧原子数为0.2 NA | |
| B. | 假设1mol氯化铁完全转化为氢氧化铁胶体,则分散系中胶体微粒数为NA | |
| C. | 60g冰醋酸中,所含阴、阳离子总数为2NA | |
| D. | 标准状况下,3.36L乙烷中含有的非极性键数为1.05NA |
查看答案和解析>>
科目: 来源: 题型:解答题
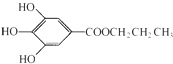 ,是白色粉末,难溶于水,微溶于棉子油等油脂,是常用的食用油抗氧化剂.
,是白色粉末,难溶于水,微溶于棉子油等油脂,是常用的食用油抗氧化剂.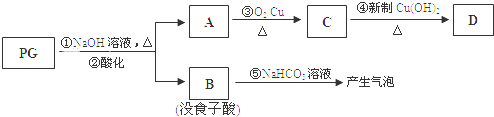
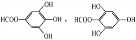
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | pH=5.6的由CH3COOH与CH3COONa组成的混合溶液中:c(Na+)>c(CH3C00-) | |
| B. | 将PH=a的醋酸稀释为pH=a+1的过程中,C(OH-)不断增大 | |
| C. | 等体积pH=a的盐酸与pH=b的氨水溶液恰好中和时,a+b=14 | |
| D. | 浓度均为0.1 mol•L-1的CH3COOH溶液和氨水等体积混合后:c(CH3COO-)+c(H+)=c(NH4+)+c(OH-) |
查看答案和解析>>
科目: 来源: 题型:解答题
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量g | 0.255 | 0.385 | 0.459 |
| 生成气体体积/mL | 280 | 336 | 336 |
查看答案和解析>>
科目: 来源: 题型:解答题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com