
科目: 来源: 题型:选择题
| A. | 常温常压下,32gO2和O3的混合气体中含有的氧原子数为2NA | |
| B. | 常温常压下,1mol氦气含有的核外电子数为4NA | |
| C. | 0.1 mol•L-1稀硫酸中硫酸根离子个数为0.1 NA | |
| D. | 22gCO2与11.2LHCl含有相同的分子数 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 等于24s | B. | 等于20s | C. | 大于20s | D. | 小于20s |
查看答案和解析>>
科目: 来源: 题型:选择题
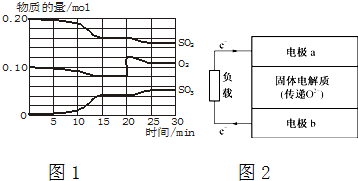
| A. | 生成SO3为2 mol | |
| B. | 反应放出197 kJ 的热量 | |
| C. | SO2和SO3物质的量之和一定为2mol | |
| D. | SO2的物质的量和SO3物质的量一定相等 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 最高正价B<A=C | |
| B. | A、B形成的化合物中只含有离子键,A、C形成的化合物中只含有共价键 | |
| C. | A、B、C三种元素能组成两种不同的化合物 | |
| D. | A、C形成的一种化合物既有氧化性又有还原性 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 化学键既存在于相邻原子间又存在于相邻分子间 | |
| B. | 两个原子间的相互作用叫化学键 | |
| C. | 化学键通常指的是相邻的两个或多个原子之间的强烈的相互作用 | |
| D. | 化学键的实质是静电吸引 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ②④⑤ | B. | ①③④ | C. | ①②③④ | D. | ①②③④⑤ |
查看答案和解析>>
科目: 来源: 题型:选择题

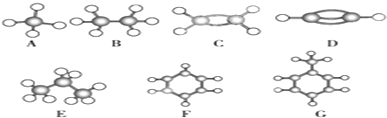
| A. | “辛烷值”可用来表示汽油的质量,异辛烷的爆震程度最小.图1是异辛烷的球棍模型,系统命名为2,4,4三甲基戊烷 | |
| B. | 用酒精萃取溴水中的溴单质的操作可选用分液漏斗,而后静置分液 | |
| C. | 乙酸乙酯中除去乙酸:用饱和碳酸钠溶液洗涤后分液 | |
| D. | 图2化合物核磁共振氢谱图中有5个吸收峰 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com