
科目: 来源: 题型:解答题


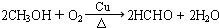 .
.查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 植物油和裂化汽油都能使溴水褪色 | B. | 食用植物油是人体的营养物质 | ||
| C. | 汽油、煤油、卤代烃均为烃 | D. | 甲醛可大量用作食品防腐剂 |
查看答案和解析>>
科目: 来源: 题型:填空题
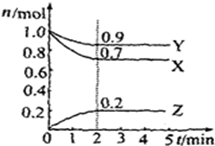 某温度时,在2L容器中X、Y、Z三种气体物质的物质的量(n)随着时间(t)变化的曲线如图所示.由图中数据分析:
某温度时,在2L容器中X、Y、Z三种气体物质的物质的量(n)随着时间(t)变化的曲线如图所示.由图中数据分析:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 乙酸与碳酸钠溶液反应:2H++CO32-=CO2↑+H2O | |
| B. | 甲醛与足量新制Cu(OH)2浊液反应:HCHO+2Cu(OH)2$\stackrel{△}{→}$HCOOH+Cu2O↓+2H2O | |
| C. | 实验室用液溴和苯在催化剂作用下制溴苯: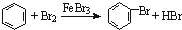 | |
| D. | 将CO2通入苯酚钠溶液: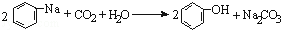 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 除去溴苯中的溴单质用氢氧化钠溶液 | |
| B. | 除去硝基苯中的二氧化氮用氢氧化钠溶液 | |
| C. | 除去甲烷中的乙烯用酸性高锰酸钾溶液 | |
| D. | 除去苯中的苯酚用氢氧化钠溶液 |
查看答案和解析>>
科目: 来源: 题型:填空题
| 实验 序号 |  | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | C3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
查看答案和解析>>
科目: 来源: 题型:填空题
 .C、D还可形成化合物D2C2,D2C2含有的化学键是离子键、非极性共价键(或离子键、共价键).
.C、D还可形成化合物D2C2,D2C2含有的化学键是离子键、非极性共价键(或离子键、共价键).查看答案和解析>>
科目: 来源: 题型:填空题
 已知在25℃、1.013×105Pa下,1mol氢气完全燃烧生成液态水放出285kJ的热量,请回答下列问题:
已知在25℃、1.013×105Pa下,1mol氢气完全燃烧生成液态水放出285kJ的热量,请回答下列问题:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 分离出少量氮化硅 | B. | 降低温度 | ||
| C. | 充入氮气 | D. | 充入氦 |
查看答案和解析>>
科目: 来源: 题型:解答题
 如图是一类甲烷燃烧电池示意图.
如图是一类甲烷燃烧电池示意图.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com